题目内容
3.下列离子方程式书写正确的是( )| A. | 用FeCl3溶液腐蚀铜电路板:Fe3++Cu═Fe2++Cu2+ | |
| B. | 水玻璃中加入稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ | |
| C. | 在氯化铝溶液中滴加过量的氨水:Al3++3 OH-═Al (OH)3↓ | |
| D. | 大理石与盐酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
分析 A.电荷不守恒;
B.硅酸钠为可溶性盐,拆成离子形式;
C.一水合氨为弱碱,应保留化学式;
D.二者反应生成氯化钙和二氧化碳、水;
解答 解:A.用FeCl3溶液腐蚀铜电路板,离子方程式:2Fe3++Cu═2Fe2++Cu2+,故A错误;
B.水玻璃中加入稀盐酸,离子方程式:SiO32-+2H+═H2SiO3↓,故B错误;
C.在氯化铝溶液中滴加过量的氨水,反应生成氢氧化铝沉淀,反应的离子方程式为:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故C错误;
D.大理石与盐酸反应,离子方程式:CaCO3+2H+═Ca2++H2O+CO2↑,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
14.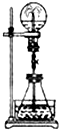 喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )
喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )
 喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )
喷泉实验是一种常见的自然现象,其产生原因是存在压强差.在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )| A. | Cu与稀盐酸 | B. | NH4HCO3与稀盐酸 | ||
| C. | CaCO3与稀硫酸 | D. | NaHCO3与NaOH溶液 |
11.用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如图,它属于( )

| A. | 无机物 | B. | 单质 | C. | 高分子化合物 | D. | 有机物 |
18.昆仑玉常用于制作奖牌等纪念品,其主要成分是由“透闪石”和“阳起石”组成的纤维状微晶结合体,其中透闪石的化学成分为Ca2Mg5Si8O22(OH)2.下列有关说法不正确的是( )
| A. | Ca2Mg5Si8O22(OH)2属于硅酸盐 | |
| B. | 昆仑玉是混合物,透闪石中Mg元素与Ca元素的质量比是3:2 | |
| C. | 透闪石的化学式写成氧化物的形式为:2CaO•5MgO•8SiO2•H2O | |
| D. | 透闪石是一种新型无机非金属材料,易溶于水 |
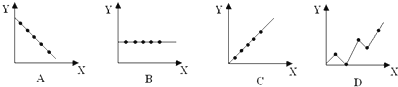
12.以极性键结合的多原子分子,分子是否有极性取决于分子的空间构型.下列分子属极性分子的是( )
| A. | SO3 | B. | CO2 | C. | NH3 | D. | BCl3 |
13.某校化学兴趣小组用如图所示过程除去AlCl3溶液中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失.

下列说法正确的是( )

下列说法正确的是( )
| A. | NaOH溶液可以用氨水来代替 | |
| B. | 沉淀a为NaAlO2 | |
| C. | 溶液b中只含有NaCl | |
| D. | 向溶液a中滴加盐酸需控制溶液的pH |
 .
.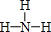 .
.
 NOx是汽车尾气中的主要污染物之一.通过NOx传感器可监测NOx的含量,其工作原理如图:
NOx是汽车尾气中的主要污染物之一.通过NOx传感器可监测NOx的含量,其工作原理如图: