题目内容
(1)由地壳中含量最高的金属元素和非金属组成的化合物的化学式是
(2)铁红常用于制造红色油漆和涂料.完成用废铁屑制备铁红的有关化学方程式:
①Fe+2HCl→FeCl2+H2↑ ②FeCl2+2NaOH→Fe(OH)2↓+2NaCl
③
(3)判断存放的FeCl2溶液是否因氧化而变质.从现象观察看
Al2O3
Al2O3
,该物质与氢氧化钠反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O
Al2O3+2OH-═2AlO2-+H2O
(2)铁红常用于制造红色油漆和涂料.完成用废铁屑制备铁红的有关化学方程式:
①Fe+2HCl→FeCl2+H2↑ ②FeCl2+2NaOH→Fe(OH)2↓+2NaCl
③
4Fe(OH)2+O2+2H2O═4Fe(OH)3↓
4Fe(OH)2+O2+2H2O═4Fe(OH)3↓
④2Fe(OH)3
Fe2O3+3H2O
| ||
2Fe(OH)3
Fe2O3+3H2O
| ||
(3)判断存放的FeCl2溶液是否因氧化而变质.从现象观察看
颜色变黄
颜色变黄
;鉴定的方法为加入KSCN溶液
KSCN溶液
试剂,若溶液出现血红色
血红色
;则证明有Fe3+
Fe3+
存在,鉴定反应的离子方程式Fe3++3SCN-?Fe(SCN)3
Fe3++3SCN-?Fe(SCN)3
.分析:(1)由地壳中含量最高的金属元素为铝和非金属元素为氧组成的化合物的化学式是Al2O3;氧化铝是两性氧化物和强酸强碱反应;
(2)制备铁红是利用氢氧化铁加热分解生成,所以生成的氢氧化亚铁氧化为氢氧化铁,受热分解得到;
(3)依据亚铁盐溶液呈淡绿色,三价铁盐溶液呈棕黄色;铁离子检验用硫氰酸钾溶液遇三价铁离子变血红色检验.
(2)制备铁红是利用氢氧化铁加热分解生成,所以生成的氢氧化亚铁氧化为氢氧化铁,受热分解得到;
(3)依据亚铁盐溶液呈淡绿色,三价铁盐溶液呈棕黄色;铁离子检验用硫氰酸钾溶液遇三价铁离子变血红色检验.
解答:解:(1)由地壳中含量最高的金属元素为铝和非金属元素为氧组成的化合物的化学式是Al2O3;氧化铝是两性氧化物和强酸强碱反应;反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al2O3;Al2O3+2OH-═2AlO2-+H2O;
(2)制备铁红是利用氢氧化铁加热分解生成,所以生成的氢氧化亚铁氧化为氢氧化铁,受热分解得到,发生的反应的化学方程式为③4Fe(OH)2+O2+2H2O═4Fe(OH)3↓;④2Fe(OH)3
Fe2O3+3H2O,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3↓;2Fe(OH)3
Fe2O3+3H2O;
(3)从现象观察看颜色变黄,则存放的FeCl2溶液因氧化而变质;加入KSCN溶液试剂,若溶液出现血红色;则证明有Fe3+ 存在,鉴定反应的离子方程式:Fe3++3SCN-?F e(SCN)3,
故答案为:颜色变黄;KSCN溶液;血红色;Fe3+;Fe3++3SCN-?F e(SCN)3.
故答案为:Al2O3;Al2O3+2OH-═2AlO2-+H2O;
(2)制备铁红是利用氢氧化铁加热分解生成,所以生成的氢氧化亚铁氧化为氢氧化铁,受热分解得到,发生的反应的化学方程式为③4Fe(OH)2+O2+2H2O═4Fe(OH)3↓;④2Fe(OH)3
| ||
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3↓;2Fe(OH)3
| ||
(3)从现象观察看颜色变黄,则存放的FeCl2溶液因氧化而变质;加入KSCN溶液试剂,若溶液出现血红色;则证明有Fe3+ 存在,鉴定反应的离子方程式:Fe3++3SCN-?F e(SCN)3,
故答案为:颜色变黄;KSCN溶液;血红色;Fe3+;Fe3++3SCN-?F e(SCN)3.
点评:本题考查了铁及其化合物性质的应用,主要是离子检验方法的分析判断,化学方程式的书写,熟练掌握基础是解题关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

 (化学方程式)
(化学方程式) 
 。
。
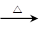 (化学方程式)
。
(化学方程式)
。