题目内容
19.实验室常用MnO2与浓盐酸共热制取C12,也可用KClO3、KMnO4、K2Cr2O7代替MnO2与浓盐酸反应制Cl2,其中KClO3→Cl2 KMnO4→Mn2+ K2Cr2O7→Cr3+.若制取等量的Cl2,电子转移数最少是( )| A. | MnO2 | B. | KClO3 | C. | KMnO4 | D. | K2Cr2O7 |
分析 KMnO4、K2Cr2O7、MnO2、KClO3与浓盐酸反应的化学方程式为:
①2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,
②K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O,
③MnO2+4HCl$\frac{\underline{\;加热\;}}{\;}$MnCl2+Cl2↑+2H2O,
④KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,
根据电荷守恒,制取等量的氯气,①②③反应中转移的电子数相等,④中注意的电子最少.
解答 解:KMnO4、K2Cr2O7、MnO2、KClO3与浓盐酸反应的化学方程式为:
①2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O,
②K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O,
③MnO2+4HCl$\frac{\underline{\;加热\;}}{\;}$MnCl2+Cl2↑+2H2O,
④KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,
设制取1mol氯气,根据电荷守恒,制取1mol氯气,①②③反应中转移了2mol电子;
④中生成3mol氯气转移了5mol电子,则生成nmol氯气转移的电子的物质的量为:$\frac{5}{3}$mol,
所以制取等量的Cl2,转移电子数最少的是KClO3,
故选B.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,注意元素化合价的判断,为解答该题的关键,从元素化合价的角度解答该类题目,难度不大.

练习册系列答案
相关题目
9.分析下列各项结构的规律,按此规律排布第8项的分子式应为( )
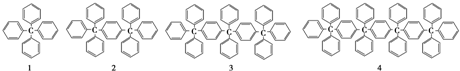

| A. | C158H118 | B. | C158H116 | C. | C160H116 | D. | C160H118 |
10.设想你采集了某星球上十种元素单质的样品,为了确定这些元素的相对位置以便系统地进行研究,你设计了一些实验并得到下列结果:
按照元素性质的周期性递变规律,试确定以上十种元素的相对位置,将其余五种元素填入下表:
| 单质 | A | B | C | D | E | F | G | H | I | J |
| 熔点(℃ | -150 | 550 | 160 | 210 | -50 | 370 | 450 | 300 | 260 | 250 |
| 与水反应 | ∨ | ∨ | ∨ | ∨ | ||||||
| 与酸反应 | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ||||
| 与氧气反应 | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ∨ | ||
| 不发生化学反应 | ∨ | ∨ | ||||||||
| 相对于A元素的原子质量 | 1.0 | 8.0 | 15.6 | 17.1 | 23.8 | 31.8 | 20.0 | 29.6 | 3.9 | 18.0 |
| A | ||||||||||
| I | B | |||||||||
| J | ||||||||||
| H | ||||||||||
7.下列叙述正确的是(用NA代表阿伏加德罗常数的值)( )
| A. | 2.4g金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 | |
| C. | 6.4g铜与足量的硫磺在绝隔空气的条件下反应,电子转移的数目为0.1NA | |
| D. | 1mol白磷分子中所含共价键数为4NA |
14.向饱和澄清石灰水中加入生石灰,再恢复到原温度,下列说法正确的是( )
| A. | Ca2+浓度减小 | B. | 溶剂质量减小 | C. | 溶液质量不变 | D. | Ca2+数目增多 |
11.对图两种化合物的结构或性质描述错误的是( )
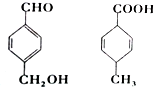

| A. | 均可以发生加成和取代反应 | |
| B. | 均能使酸性高锰酸钾溶液褪色 | |
| C. | 互为同分异构体 | |
| D. | 既能用红外光谱区分,也可以用核磁共振氢谱区分 |
8.下列选项不正确的是( )
| A. | 从碘水中提取碘的方法是萃取 | |
| B. | 物质的量浓度的单位是mol/L | |
| C. | 胶体与溶液的本质区别是丁达尔效应 | |
| D. | 氧化还原反应的实质是电子的转移 |
9.下列气体对呼吸道有刺激作用的是( )
| A. | O2 | B. | N2 | C. | CO2 | D. | NH3 |
 .
.