题目内容
用NA表示阿伏加德罗常数的值.下列判断错误的是( )
| A、NA个H+的质量为1 g |
| B、2 L 0.5 mol/L Na2SO4溶液中含2NA个Na+ |
| C、32 g O2中含有2NA个O原子 |
| D、标准状况下,22.4 L CCl4中含有NA个分子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氢离子的摩尔质量为1g/mol,NA个H+的物质的量为1mol,质量为1g;
B.根据n=cV计算出硫酸钠的物质的量,再计算出含有钠离子的物质的量及数目;
C.32g氧气的物质的量为1mol,1mol氧气含有2mol氧原子;
D.标准状况下,四氯化碳的状态不是气体,不能使用标况下的气体摩尔体积计算其物质的量.
B.根据n=cV计算出硫酸钠的物质的量,再计算出含有钠离子的物质的量及数目;
C.32g氧气的物质的量为1mol,1mol氧气含有2mol氧原子;
D.标准状况下,四氯化碳的状态不是气体,不能使用标况下的气体摩尔体积计算其物质的量.
解答:
解:A.NA个H+的物质的量为1mol,1mol氢离子的质量为1g,故A正确;
B.2 L 0.5 mol/L Na2SO4溶液中含有1mol硫酸钠,含有2mol钠离子,溶液中含2NA个Na+,故B正确;
C.32g氧气的物质的量为1mol,含有2mol氧原子,含有2NA个O原子,故C正确;
D.标况下四氯化碳不是气体,不能使用标况下的气体摩尔体积计算22.4L四氯化碳的物质的量,故D错误;
故选D.
B.2 L 0.5 mol/L Na2SO4溶液中含有1mol硫酸钠,含有2mol钠离子,溶液中含2NA个Na+,故B正确;
C.32g氧气的物质的量为1mol,含有2mol氧原子,含有2NA个O原子,故C正确;
D.标况下四氯化碳不是气体,不能使用标况下的气体摩尔体积计算22.4L四氯化碳的物质的量,故D错误;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下四氯化碳、乙醇、水等不是去,要求掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
用VSEPR模型预测,下列分子形状与H2O相似,都为V型的是( )
| A、OF2 |
| B、BeCl2 |
| C、SO2 |
| D、CO2 |
氮化钠(Na3N)熔融时能导电,与水作用产生NH3.下列对氮化钠晶体描述错误的是( )
| A、构成晶体的两种微粒电子层结构相同 |
| B、构成晶体的两种微粒半径不相等 |
| C、与盐酸反应生成盐的化学键类型相同 |
| D、与盐酸反应生成盐的晶体类型相同 |
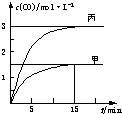 一定条件下存在反应:C(s)+H2O(g)?CO(g)+H2(g)△H>0.向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示.
一定条件下存在反应:C(s)+H2O(g)?CO(g)+H2(g)△H>0.向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示.| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | V |
| 温度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2mol C、1mol H2O | 1mol CO、1mol H2 | 4mol C、2mol H2O |
| A、甲容器中,反应在前15 min的平均速率v(H2)=0.01 mol?L-1?min-1 |
| B、丙容器的体积V<0.5 L |
| C、当温度为T1℃时,反应的平衡常数K=2.25 |
| D、乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2 |
某有机化合物的结构简式为 它可以发生的反应类型有( )
它可以发生的反应类型有( )
a取代 b加成 c消去 d酯化 e水解 f中和 g缩聚 h加聚.
 它可以发生的反应类型有( )
它可以发生的反应类型有( )a取代 b加成 c消去 d酯化 e水解 f中和 g缩聚 h加聚.
| A、acdf | B、befh |
| C、abcd | D、除eh外 |
用图示装置(试剂任选)能完成下列实验的是( )
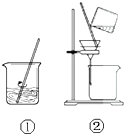

| A、从粗盐中获得NaCl晶体 |
| B、除去附着在铁屑表面的铝 |
| C、从含苯酚的废水中回收苯酚 |
| D、除去Fe(OH)3胶体中的FeCl3 |
NA为阿伏加德罗常数,下列说法中正确的是( )
| A、17gNH4+中含有的电子数为10NA |
| B、1mol?L-1Mg(NO3)2溶液中含有NO3-的数目为2NA |
| C、标准状况下,22.4L乙醇所含的分子数为NA |
| D、室温下,28.0g乙烯和丙烯中混合气体中含有的碳原子数为2NA |
下列有关化学平衡常数K的叙述正确的是( )
| A、与反应温度有关 |
| B、与反应物性质有关 |
| C、与反应物浓度有关 |
| D、与反应物接触面积有关 |
某烷烃的相对分子质量为86,与氯气反应生成的一氯代物只有两种,其结构简式是( )
| A、CH3(CH2)4CH3 |
| B、(CH3)2CHCH(CH3)2 |
| C、(C2H5)2CHCH3 |
| D、C2H5C(CH3)3 |