题目内容
18.(1)某烃相对分子质量为84,则其分子式为C6H12,该烃能使溴水褪色,测得其核磁共振氢谱中只有一个信号峰,则其结构简式为 ,系统命名的名称为2,3-二甲基-2-丁烯.
,系统命名的名称为2,3-二甲基-2-丁烯.(2)已知烯烃和NBS作用,烯烃中与双键碳相邻碳原子上的一个氢原子被溴原子取代.分了式为C4H8的烃和NBS作用,得到的一溴代烯烃有3种,其中有一种有顺反异构,结构简式为:顺式
 反式
反式 若用丙烯制取1,2,3-三溴丙烷,最适合的方法是先溴单质与丙烯在高温下发生α-H取代反应生成生成3-溴丙烯再让3-溴丙烯和溴单质加成,此时才能得到1,2,3-三溴丙烷.
若用丙烯制取1,2,3-三溴丙烷,最适合的方法是先溴单质与丙烯在高温下发生α-H取代反应生成生成3-溴丙烯再让3-溴丙烯和溴单质加成,此时才能得到1,2,3-三溴丙烷.
分析 (1)利用余商法计算该烃的C、H原子数,从而确定该烃的分子式;其核磁共振氢谱中只有一个吸收峰,则分子中只有一种类型的氢原子,则烃A为对称结构,进而推断结构简式并命名;
(2)分子式为C4H8的烯烃的同分异构体有3种,分别为1-丁烯、2-丁烯、2-甲基-1-丙烯,这些烯烃中与双键碳相邻碳原子上的一个氢原子被溴原子取代的产物有:CH2=CHCH(Br)CH3,CH3CH=CHCH2Br,CH2=C(CH3)CH2Br;当两个相同的原子或基团处于π键平面的同侧时称顺式异构;当处于π键平面的异侧时称反式异构;先让溴单质与丙烯取代,需加热(因为烯烃低温加成,高温取代),发生自由基型反应,生成3-溴丙烯,再让3-溴丙烯和溴单质加成,此时才能得到纯净的产物.
解答 解:(1)某烃相对分子质量为84,利用商余法,分子中最大碳原子数目为:$\frac{84}{14}$=6,含H原子为$\frac{84-12×6}{1}$=12,即该烃分子含有6个C原子、12个H原子,
所以该烃的分子式为C6H12;该有机物分子的核磁共振氢谱中只有一个吸收峰,则其分子中只有一种类型的氢,故烃A为对称结构,即双键C原子上的4个H均被甲基取代,其结构简式应为: ,名称为:2,3-二甲基-2-丁烯;
,名称为:2,3-二甲基-2-丁烯;
故答案为:C6H12; ;2,3-二甲基-2-丁烯;
;2,3-二甲基-2-丁烯;
(2)分子式为C4H8的烯烃的同分异构体有3种,分别为1-丁烯、2-丁烯、2-甲基-1-丙烯,这些烯烃中与双键碳相邻碳原子上的一个氢原子被溴原子取代的产物有:CH2=CHCH(Br)CH3,CH3CH=CHCH2Br,CH2=C(CH3)CH2Br,一溴代物共有3种;其中CH3CH=CHCH2Br有顺反异构,顺式异构为 ,反式异构为
,反式异构为 ;先让溴单质与丙烯在高温下发生α-H取代反应生成生成3-溴丙烯,再让3-溴丙烯和溴单质加成,此时才能得到1,2,3-三溴丙烷;
;先让溴单质与丙烯在高温下发生α-H取代反应生成生成3-溴丙烯,再让3-溴丙烯和溴单质加成,此时才能得到1,2,3-三溴丙烷;
故答案为:3; ;
; ;溴单质与丙烯在高温下发生α-H取代反应生成生成3-溴丙烯;再让3-溴丙烯和溴单质加成,此时才能得到1,2,3-三溴丙烷.
;溴单质与丙烯在高温下发生α-H取代反应生成生成3-溴丙烯;再让3-溴丙烯和溴单质加成,此时才能得到1,2,3-三溴丙烷.
点评 本题主要考查了有机物分子式、结构简式的确定,烯烃的性质等,题目难度中等,明确常见有机物结构与性质为解答关键,试题侧重考查学生的分析能力及化学计算能力.

| A. | 3s10 | B. | 3d10 | C. | 3s23p63d2 | D. | 3s23p53d3 |
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③熔点:SO3>SiO2>CO2
④结合质子能力:OH->CH3COO->Cl-.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
| A. | Zn为负极,Ag2O是正极 | |
| B. | 在使用过程中,电池负极区溶液的c(OH-)值减小 | |
| C. | 电池工作时,电子由Zn极经外电路流向Ag2O极 | |
| D. | 电路中每通过0.2mol电子,负极的质量理论上减少6.5g |
| A. | CH2═CH-CH2CH2CH2CH3 | B. | CH3CH2CH═CHCH2CH3 | ||
| C. | CH3CH═CHCH2CH2CH3 | D. | 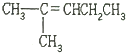 |
| A. | 冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸 | |
| C. | 漂白粉、福尔马林、冰水、王水、氯水均为混合物 | |
| D. | Na2O,NaOH,NaCl,Na2SO4,Na2O2都属于钠的含氧化合物 |
| A. | Ag+、NO3-、Cl-、K+ | B. | Na+、Fe2+、Cl-、NO3- | ||
| C. | K+、Ba2+、OH-、SO42- | D. | Cu2+、NH4+、Br-、Cl- |
