题目内容
1.常温时,下列事实一定能证明HA是弱酸的是( )| A. | 用HA溶液做导电实验,灯泡很暗 | |
| B. | HA和CaCO3发生反应放出CO2 | |
| C. | pH=2的HA溶液稀释至100倍,pH小于4 | |
| D. | pH=3的HA溶液中水电离出的c(H+)为10-11mol•L-1 |
分析 要证明一元酸HR为弱酸,可证明存在电离平衡、不能完全电离或从对应的强碱盐溶液呈碱性的角度,以此解答该题.
解答 解:A.用HA溶液做导电实验,灯泡很暗,说明该溶液中离子浓度较低,但不能说明HA部分电离,所以不能证明HA是弱酸,故A错误;
B.HA能和碳酸钙反应生成二氧化碳说明HA酸性大于碳酸,但不能说明HA部分电离,所以不能证明HA是弱酸,故B错误;
C.pH=2的HA溶液稀释至100倍,pH小于4,说明稀释过程中HA发生电离,则HA为弱电解质,故C正确;
D.常温下,无论HA是强酸还是弱酸,pH=3的HA溶液中水电离出的c(H+)=c(OH-)=10-11mol•L-1,不能说明HA部分电离,所以不能证明HA是弱酸,故D错误;
故选C.
点评 本题考查强弱电解质的判断,为高频考点,强弱电解质的根本区别是电离程度,与物质溶解性强弱、溶液导电性强弱无关,为易错题.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
11.下列事实不能用勒夏特列原理解释的是( )
| A. | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | |
| B. | 钢铁在潮湿的空气中容易生锈 | |
| C. | 工业上生产硫酸的过程中,二氧化硫在接触室氧化时通入过量空气(O2) | |
| D. | 工业合成氨时常用通过量氮气的方法提高氢气的转化率 |
12.已知硫酸亚铁溶液中加入过氧化钠时发生反应:4Fe2++4Na2O2+6H2O═4Fe(OH)3↓+O2↑+8Na+,则下列说法正确的是( )
| A. | 该反应中Fe2+是还原剂,O2是还原产物 | |
| B. | 4 mol Na2O2在反应中共得到8NA个电子 | |
| C. | 每生成4 mol Fe(OH)3反应过程中共转移电子6 mol | |
| D. | 反应过程中可以看到白色沉淀转化为灰绿色再转化为红褐色沉淀 |
9.黑火药爆炸时可发生如下反应:5S+16KNO3+16C=3K2SO4+4K2CO3+K2S+12CO2↑+8N2↑,下列有关说法正确的是( )
| A. | S既作氧化剂又作还原剂 | B. | 消耗12gC时,反应转移5mol电子 | ||
| C. | 还原产物只有K2S | D. | KNO3只发生氧化反应 |
16.下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是( )
| A. | 半导体材料碳化硅 | B. | 超导材料铜锌合金 | ||
| C. | 透明陶瓷材料硒化锌 | D. | 超导材料Cs3C60 |
13.已知室温时,0.1mo1/L某一元酸HX有0.1%发生电离,下列叙述错误的是( )
| A. | 该溶液的pH=4 | |
| B. | 适当升高温度,溶液的pH不变 | |
| C. | 此酸的电离平衡常数约为1×10-7 | |
| D. | 由HX电离出的c(H+)约为水电离出的c(OH-)的106倍 |
 ,A的名称是2-甲基戊烷. 若A是炔烃B氢化而成,则B的结构有2种
,A的名称是2-甲基戊烷. 若A是炔烃B氢化而成,则B的结构有2种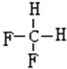 和
和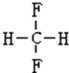 F.
F.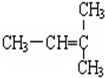 和
和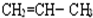 G.
G.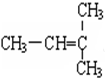 和
和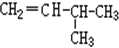

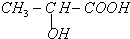 ,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
 .
.