题目内容
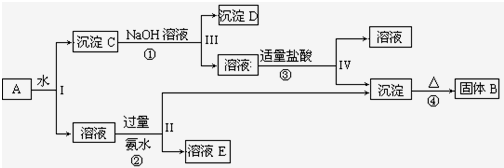
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是 .
(2)根据上述框图反应关系,写出下列B、D所含物质的化学式.固体B ;沉淀D .
(3)写出①、②反应的离子方程式:① ;② .
(4)以Fe2O3为原料,可制备FeCl2溶液,请写出有关的化学反应方程式,试剂任选 .

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出下列B、D所含物质的化学式.固体B
(3)写出①、②反应的离子方程式:①
(4)以Fe2O3为原料,可制备FeCl2溶液,请写出有关的化学反应方程式,试剂任选
考点:物质分离和提纯的方法和基本操作综合应用
专题:化学实验基本操作
分析:某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,加水后经过滤分离可得溶液KAl(SO4)2和Al2O3、Fe2O3沉淀混合物C,加入NaOH溶液,NaOH和Al2O3反应生成NaAlO2,过滤后得到NaAlO2溶液,沉淀D为Fe2O3,加入盐酸得到FeCl3,NaAlO2溶液中加入适量盐酸,反应生成Al(OH)3和NaCl,Al(OH)3加热分解生成B为Al2O3,溶液E为K2SO4和(NH4)2SO4混合物,
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是过滤;
(2)由以上分析可知B为Al2O3,D为Fe2O3,;
(3)反应①为Al2O3和氢氧化钠的反应,反应②为Al3+和氨水的反应;
(4)以Fe2O3为原料,可制备FeCl2溶液,先用盐酸溶解得到氯化铁溶液,加入过量铁粉还原得到氯化亚铁.
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是过滤;
(2)由以上分析可知B为Al2O3,D为Fe2O3,;
(3)反应①为Al2O3和氢氧化钠的反应,反应②为Al3+和氨水的反应;
(4)以Fe2O3为原料,可制备FeCl2溶液,先用盐酸溶解得到氯化铁溶液,加入过量铁粉还原得到氯化亚铁.
解答:
解:某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,加水后经过滤分离可得溶液KAl(SO4)2和Al2O3、Fe2O3沉淀混合物C,加入NaOH溶液,NaOH和Al2O3反应生成NaAlO2,过滤后得到NaAlO2溶液,沉淀D为Fe2O3,加入盐酸得到FeCl3,NaAlO2溶液中加入适量盐酸,反应生成Al(OH)3和NaCl,Al(OH)3加热分解生成B为Al2O3,溶液E为K2SO4和(NH4)2SO4混合物,
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是过滤,故答案为:过滤;
(2)由以上分析可知B为Al2O3,D为Fe2O3,故答案为:Al2O3;Fe2O3;
(3)反应①为Al2O3和氢氧化钠的反应,离子方程式为Al2O3+2OH-=2AlO2-+H2O,反应②为Al3+和氨水的反应,反应的离子方程式为Al3++3NH3、H2O=Al(OH)3↓+3 NH4+;
故答案为:Al2O3+2OH-=2AlO2-+H2O;Al3++3NH3?H2O=Al(OH)3↓+3 NH4+;
(4)以Fe2O3为原料,可制备FeCl2溶液,先用盐酸溶解得到氯化铁溶液,加入过量铁粉还原得到氯化亚铁,反应的化学方程式为:Fe2O3+6HCl=2 FeCl3+3 H2O;2FeCl3+Fe=3FeCl2 ;
故答案为:Fe2O3+6HCl=2 FeCl3+3 H2O、2FeCl3+Fe=3FeCl2 .
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是过滤,故答案为:过滤;
(2)由以上分析可知B为Al2O3,D为Fe2O3,故答案为:Al2O3;Fe2O3;
(3)反应①为Al2O3和氢氧化钠的反应,离子方程式为Al2O3+2OH-=2AlO2-+H2O,反应②为Al3+和氨水的反应,反应的离子方程式为Al3++3NH3、H2O=Al(OH)3↓+3 NH4+;
故答案为:Al2O3+2OH-=2AlO2-+H2O;Al3++3NH3?H2O=Al(OH)3↓+3 NH4+;
(4)以Fe2O3为原料,可制备FeCl2溶液,先用盐酸溶解得到氯化铁溶液,加入过量铁粉还原得到氯化亚铁,反应的化学方程式为:Fe2O3+6HCl=2 FeCl3+3 H2O;2FeCl3+Fe=3FeCl2 ;
故答案为:Fe2O3+6HCl=2 FeCl3+3 H2O、2FeCl3+Fe=3FeCl2 .
点评:本题考查混合物分离实验,综合考查学生的分析能力和实验能力,为高考常见题型和高频考点,注意根据物质的性质把握转化关系,难度中等,注意把握离子的检验方法和相关方程式的书写.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
假定C2H6与Cl2发生取代反应时,各种产物均可能生成,则生成物最多有( )
| A、8种 | B、9种 |
| C、10种 | D、11种 |
下列应用或事实没有体现出胶体的性质的是( )
| A、用明矾净化饮用水 |
| B、清晨林间透过缕缕阳光 |
| C、三氯化铁溶液中加入NaOH出现红褐色沉淀 |
| D、向煮熟的豆浆中加入石膏或卤水以生产豆腐 |
下列电离方程式错误的是( )
| A、NaHSO4═Na++H++SO42- |
| B、NaHCO3═Na++H++CO32- |
| C、MgCl2═Mg2++2Cl- |
| D、Ba(OH)2═Ba2++2OH- |
下列各组有机物中,只用一种试剂无法鉴别的是( )
| A、苯、苯酚、己烯 |
| B、苯、甲苯、乙苯 |
| C、乙醇、甲苯、硝基苯 |
| D、乙醇、乙醛、乙酸 |
 有机物A、B、C、D、E能发生如图所示的转化,其中C、D是生活中常见的有机物,E是具有特殊香味且不溶于水的液体.请回答下面有关问题:
有机物A、B、C、D、E能发生如图所示的转化,其中C、D是生活中常见的有机物,E是具有特殊香味且不溶于水的液体.请回答下面有关问题: