题目内容
加碘食盐中含有的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解.在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应.工业生产碘酸钾的流程如下:
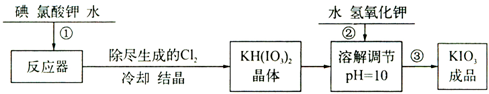
(1)步骤②中氢氧化钾的主要作用是 .
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,可经过 、过滤、洗涤、干燥等步骤.
(3)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32-=2I-+S4O62-
为了测定加碘食盐中碘的含量,某学生设计了如下实验:准确称取wg食盐,加适量蒸馏水使其完全溶解;再用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;最后加入指示剂,以物质的量浓度为2.00×10-3mol?L-1的Na2S2O3溶液滴定,消耗10.00mL时恰好反应完全.
①在滴定过程中,所用的玻璃仪器为 、 .
②该实验可以用 作指示剂,滴定终点的现象是 .
③下列有关该滴定实验的说法不正确的是 .
A.滴定管在使用前必须检查是否漏水并润洗
B.滴定时眼睛注视滴定管内溶液液面变化
C.为减小实验误差,可用少量的蒸馏水冲洗锥形瓶内壁
D.终点读数时俯视会导致碘的含量偏低
④加碘食盐样品中的碘元素含量是 g?kg-1(以含w的代数式表示).

(1)步骤②中氢氧化钾的主要作用是
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,可经过
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3/100g水 | 8.08 | 12.6 | 18.3 | 24.8 |
为了测定加碘食盐中碘的含量,某学生设计了如下实验:准确称取wg食盐,加适量蒸馏水使其完全溶解;再用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;最后加入指示剂,以物质的量浓度为2.00×10-3mol?L-1的Na2S2O3溶液滴定,消耗10.00mL时恰好反应完全.
①在滴定过程中,所用的玻璃仪器为
②该实验可以用
③下列有关该滴定实验的说法不正确的是
A.滴定管在使用前必须检查是否漏水并润洗
B.滴定时眼睛注视滴定管内溶液液面变化
C.为减小实验误差,可用少量的蒸馏水冲洗锥形瓶内壁
D.终点读数时俯视会导致碘的含量偏低
④加碘食盐样品中的碘元素含量是
考点:物质分离和提纯的方法和基本操作综合应用,中和滴定
专题:实验设计题
分析:(1)碘酸氢钾可与氢氧化钾反应生成碘酸钾;
(2)由表中数据可知温度越高,KIO3溶解度越大,从溶液中获得晶体需要蒸发结晶;
(3)①Na2S2O3溶液呈碱性,使用碱性滴定管;
②该实验产生碘单质,可以淀粉溶液作指示剂;
③A、滴定管应该是先用蒸馏水润洗,然后用待测液润洗;
B、滴定时,眼睛注视着锥形瓶中溶液的颜色变化;
C、用蒸馏水冲洗锥形瓶内壁,可冲洗附在锥形瓶内壁上的待测液,以减小实验误差;
D、终点读数时俯视会导致碘的含量偏低;
④根据硫代硫酸钠与碘酸钾的关系式计算碘酸钾的物质的量,再根据质量分数公式计算碘的含量.
(2)由表中数据可知温度越高,KIO3溶解度越大,从溶液中获得晶体需要蒸发结晶;
(3)①Na2S2O3溶液呈碱性,使用碱性滴定管;
②该实验产生碘单质,可以淀粉溶液作指示剂;
③A、滴定管应该是先用蒸馏水润洗,然后用待测液润洗;
B、滴定时,眼睛注视着锥形瓶中溶液的颜色变化;
C、用蒸馏水冲洗锥形瓶内壁,可冲洗附在锥形瓶内壁上的待测液,以减小实验误差;
D、终点读数时俯视会导致碘的含量偏低;
④根据硫代硫酸钠与碘酸钾的关系式计算碘酸钾的物质的量,再根据质量分数公式计算碘的含量.
解答:
解:(1)KH(IO3)2可与KOH反应生成KIO3,反应的方程式为KH(IO3)2+KOH═2KIO3+H2O,故答案为:与KH(IO3)2反应使其转化为KIO3;
(2)由表中数据可知温度越高,KIO3溶解度越大,从溶液中获得KIO3晶体需要蒸发结晶,故答案为:蒸发结晶;
(3)①在滴定过程中,所用的玻璃仪器为滴定管和锥形瓶,Na2S2O3溶液呈碱性,使用碱性滴定管,故答案为:碱式滴定管;锥形瓶;
②该实验产生碘单质,可以淀粉溶液作指示剂,溶液的蓝色消失且半分钟内不再变化达到滴定终点,故答案为:淀粉溶液;溶液的蓝色消失且半分钟内不再变化;
③A、滴定管应该是先检查是否漏水,然后用蒸馏水润洗,最后用待测液润洗,故A正确;
B、滴定时眼睛注视着锥形瓶中溶液的颜色变化,以便及时判断滴定终点,故B错误;
C、用蒸馏水冲洗锥形瓶内壁,可冲洗附在锥形瓶内壁上的待测液,以减小实验误差,故C正确;
D、终点读数时俯视会导致碘的含量偏低,故D正确;
故答案为:B
④设碘酸钾的物质的量为x.
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O①; I2+2S2O3 2-=2I-+S4 O62-②,将方程式②×3+①得
IO3-+6H++6S2O32-=I-+3S4O62-+3H2O
1 6
x 2.0×10-3mol/L×0.01L
x=
=
×10-5mol,
根据碘原子守恒知,碘元素的质量=
×10-5mol×127g/mol=4.23×10-4g,所以碘元素的质量分数=
×100%=
g/kg,
故答案为:
.
(2)由表中数据可知温度越高,KIO3溶解度越大,从溶液中获得KIO3晶体需要蒸发结晶,故答案为:蒸发结晶;
(3)①在滴定过程中,所用的玻璃仪器为滴定管和锥形瓶,Na2S2O3溶液呈碱性,使用碱性滴定管,故答案为:碱式滴定管;锥形瓶;
②该实验产生碘单质,可以淀粉溶液作指示剂,溶液的蓝色消失且半分钟内不再变化达到滴定终点,故答案为:淀粉溶液;溶液的蓝色消失且半分钟内不再变化;
③A、滴定管应该是先检查是否漏水,然后用蒸馏水润洗,最后用待测液润洗,故A正确;
B、滴定时眼睛注视着锥形瓶中溶液的颜色变化,以便及时判断滴定终点,故B错误;
C、用蒸馏水冲洗锥形瓶内壁,可冲洗附在锥形瓶内壁上的待测液,以减小实验误差,故C正确;
D、终点读数时俯视会导致碘的含量偏低,故D正确;
故答案为:B
④设碘酸钾的物质的量为x.
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O①; I2+2S2O3 2-=2I-+S4 O62-②,将方程式②×3+①得
IO3-+6H++6S2O32-=I-+3S4O62-+3H2O
1 6
x 2.0×10-3mol/L×0.01L
x=
| 2.0×10-3mol/L×0.01L×1 |
| 6 |
| 1 |
| 3 |
根据碘原子守恒知,碘元素的质量=
| 1 |
| 3 |
| ||
| w |
| 1.27 |
| 3w |
故答案为:
| 1.27 |
| 3w |
点评:本题是一道物质分离和提纯以及中和滴定知识的综合实验题,要求学生具有知识迁移和应用的能力,计算时注意求的是食盐中碘的含量而不是碘酸钾的含量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在2A(g)+B (g)?3C(g)+4D(g)中,表示该反应速率最快的是( )
| A、υ(A)=6.5mol?L-1?min-1 |
| B、υ(B)=0.3 mol?L-1?S-1 |
| C、υ(C)=5.4mol?L-1?min-1 |
| D、υ(D)=1 mol?L-1?S-1 |
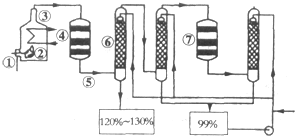 如图是现今常规生产发烟硫酸和硫酸的流程图:
如图是现今常规生产发烟硫酸和硫酸的流程图: