题目内容
1.已知:Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O.取一定质量的锌粒与10.0ml 物质的量浓度为18.5mol/L的浓硫酸充分反应,Zn完全溶解,同时生成标准状况下的SO2和H2混合气体共3.36L.将反应后的溶液稀释至1L,测得溶液中c(H+)=0.01mol/L.则混合气体中SO2和H2的体积比为1:4.分析 根据氢离子物质的量计算剩余硫酸物质的量,进而计算参加反应硫酸物质的量,设SO2和H2的物质的量分别为xmol、ymol,表示出反应消耗硫酸,再结合二者总体积列方程计算解答.
解答 解:反应后剩余氢离子为1L×0.01mol/L=0.01mol,则参加反应硫酸为0.01L×18.5mol/L-$\frac{0.01mol}{2}$=0.18mol,
设SO2和H2的物质的量分别为xmol、ymol,则:
Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O
2xmol xmol
Zn+H2SO4=ZnSO4+H2↑
ymol ymol
可得:$\left\{\begin{array}{l}{x+y=\frac{3.36}{22.4}}\\{2x+y=0.18}\end{array}\right.$
解得x=0.03、y=0.12
故混合气体中SO2和H2的体积比为0.03mol:0.12mol=1:4,
故答案为:1:4.
点评 本题考查化学方程式有关计算,难度不大,有利于基础知识的巩固.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.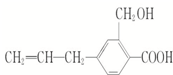 某有机物的结构简式为如右图所示,其可能具有的性质是( )
某有机物的结构简式为如右图所示,其可能具有的性质是( )
①能发生加成反应
②能使酸性高锰酸钾溶液褪色
③能发生取代反应
④能发生中和反应
⑤能发生氧化反应.
 某有机物的结构简式为如右图所示,其可能具有的性质是( )
某有机物的结构简式为如右图所示,其可能具有的性质是( ) ①能发生加成反应
②能使酸性高锰酸钾溶液褪色
③能发生取代反应
④能发生中和反应
⑤能发生氧化反应.
| A. | 全部 | B. | 仅能发生①②③④ | C. | 除⑤外都能 | D. | 除④⑤外都能 |
12.已知短周期元素的离子aW2+、bX+、cY2-、dZ-具有相同的电子层结构,下列正确的是( )
| A. | 原子序数:a>b>c>d | B. | 离子的还原性:Y2->Z- | ||
| C. | 氢化物的稳定性H2Y>HZ | D. | 原子半径X<W |
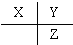
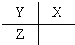
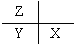

 ;B:
;B: ;G:HCOOCH3
;G:HCOOCH3 .
.