题目内容
浓硫酸、新制氯水、浓盐酸分别滴在蓝色石蕊试纸上,最终试纸的颜色分别是( )
| A、黑色、红色、红色 |
| B、红色、红色、红色 |
| C、黑色、白色、红色 |
| D、红色、白色、黑色 |
考点:浓硫酸的性质,氯气的化学性质,指示剂的使用
专题:元素及其化合物
分析:浓硫酸具有脱水性,新制氯水含有盐酸和次氯酸具有酸性和漂白性,浓盐酸具有酸性,据此解答.
解答:
解:A.浓硫酸具有脱水性,能够使石蕊试纸脱水生成碳,颜色变黑;新制氯水具有酸性和漂白性,能够使蓝色石蕊试纸先变红后褪色变白;浓盐酸具有酸性,能够使蓝色石蕊试纸变红色,
故选:C.
故选:C.
点评:本题为实验题,明确浓硫酸的脱水性、次氯酸的漂白性、盐酸的酸性,是解题关键,注意对基础知识的积累.

练习册系列答案
相关题目
同温同压下分别为0.2mol的H2O和O2,它们一定具有相同的( )
| A、体积 | B、分子数 |
| C、摩尔质量 | D、质量 |
下列事实不能用电化学理论解释的是( )
| A、轮船水线下船壳上装有一定数量的锌块 |
| B、粗锌比纯锌制H2更快 |
| C、镀锌铁比镀锡铁耐用 |
| D、银质奖章长期放置后表面会变暗 |
如图是某硫酸试剂瓶的标签上的部分信息.下列说法正确的是( )


| A、常温下,该试剂可与金属铝反应生成大量的无色气体 |
| B、1 mol Zn与足量的该硫酸反应生成2 g氢气 |
| C、该硫酸与等体积水混合所得溶液的物质的量浓度大于9.2 mol/L |
| D、向50 mL该硫酸中加入足量的铜片,加热,反应后被还原的硫酸的物质的量小于0.46 mol |
在下列各溶液中,离子一定能大量共存的是( )
| A、pH=11的溶液中:CO32-、Na+、AlO2-、NO3- |
| B、含有0.1mol?L-1Fe3+的溶液中:K+、Mg2+、I-、NO3- |
| C、无色溶液中:K+、Na+、MnO4-、SO42- |
| D、室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42- |
一定温度下,满足下列条件的溶液一定呈酸性的是( )
| A、pH<7的某物质的水溶液 |
| B、加酚酞后显无色的溶液 |
| C、能与金属Al反应放出H2的溶液 |
| D、c(H+)>c(OH-)的任意物质的水溶液 |
某同学设计了由乙醇合成乙二醇的路线如下.下列说法正确的是( )
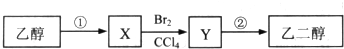

| A、X可以发生加成反应 |
| B、步骤①的反应类型是水解反应 |
| C、步骤②需要在氢氧化钠醇溶液中反应 |
| D、等物质的量的乙醇、X完全燃烧,消耗氧气的量不相同 |
1mol某气态烃与5mol氧气在密闭容器中点燃,烃和氧气全部耗尽,测得生成4mol H2O(g)、2mol CO2和2mol CO(气体体积均在同温同压下测定)该烃的分子式是( )
| A、C4H10 |
| B、C3H8 |
| C、C4H8 |
| D、C2H4 |
甲酸的下列性质中,可以证明它是弱电解质的是( )
| A、甲酸能与水以任意比互溶 |
| B、1mol/L甲酸溶液的PH约为2 |
| C、10mL1mol/L甲酸恰好与10mL1mol/LNaOH溶液完全反应 |
| D、在相同条件下,甲酸溶液的导电性比强酸溶液的弱 |