题目内容
如图是某硫酸试剂瓶的标签上的部分信息.下列说法正确的是( )


| A、常温下,该试剂可与金属铝反应生成大量的无色气体 |
| B、1 mol Zn与足量的该硫酸反应生成2 g氢气 |
| C、该硫酸与等体积水混合所得溶液的物质的量浓度大于9.2 mol/L |
| D、向50 mL该硫酸中加入足量的铜片,加热,反应后被还原的硫酸的物质的量小于0.46 mol |
考点:浓硫酸的性质
专题:元素及其化合物
分析:依据C=
计算硫酸的物质的量浓度为18.4mol/L,该硫酸为浓硫酸.
A.浓硫酸具有强的氧化性,常温下能够使铝钝化;
B.锌与浓硫酸反应不能得到氢气;
C.分子间有间隙,等体积浓硫酸与等体积水混合,体积小于二体积;
D.铜只能与浓硫酸反应,与稀硫酸不反应.
| 1000ρω |
| M |
A.浓硫酸具有强的氧化性,常温下能够使铝钝化;
B.锌与浓硫酸反应不能得到氢气;
C.分子间有间隙,等体积浓硫酸与等体积水混合,体积小于二体积;
D.铜只能与浓硫酸反应,与稀硫酸不反应.
解答:
依据C=
计算硫酸的物质的量浓度为18.4mol/L,该硫酸为浓硫酸.
解:A.浓硫酸具有强的氧化性,常温下能够使铝钝化,故A错误;
B.浓硫酸具有强的氧化性,与任何金属反应都不能生成氢气,故B错误;
C.分子间有间隙,等体积浓硫酸与等体积水混合,体积小于二体积,所以混合所得溶液的物质的量浓度大于9.2 mol/L,故C正确;
D.随着反应的进行硫酸浓度逐渐降低,铜只能与稀硫酸反应,所以反应后被还原的硫酸的物质的量小于0.46 mol,故D正确;
故选:CD.
| 1000ρω |
| M |
解:A.浓硫酸具有强的氧化性,常温下能够使铝钝化,故A错误;
B.浓硫酸具有强的氧化性,与任何金属反应都不能生成氢气,故B错误;
C.分子间有间隙,等体积浓硫酸与等体积水混合,体积小于二体积,所以混合所得溶液的物质的量浓度大于9.2 mol/L,故C正确;
D.随着反应的进行硫酸浓度逐渐降低,铜只能与稀硫酸反应,所以反应后被还原的硫酸的物质的量小于0.46 mol,故D正确;
故选:CD.
点评:本题考查了浓硫酸的性质,熟悉浓硫酸具有吸水性、脱水性、强氧化性是解题关键,注意铜只能与浓硫酸发生反应,与稀硫酸不反应.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
质量相同的氧气和二氧化碳中所含原子个数之比为( )
| A、11:8 | B、11:12 |
| C、1:1 | D、3:2 |
下列各对物质中,互为同系物的是( )
A、 |
| B、HCOOCH3与CH3CHOOH |
C、 |
| D、C6H5OH与C6H5CH2OH |
短周期元素A和B可形成AB3型化合物.若B原子序数为m,则A的原子序数为下面算式中的①m+6 ②m+4 ③m-4 ④m-2 ⑤m+8 ⑥m+14 ⑦m-12( )
| A、②③⑥ | B、①②③④ |
| C、①②⑥⑦ | D、①②③④⑤⑥⑦ |
下列说法正确的是( )
| A、能导电的物质叫电解质 |
| B、酸、碱和盐都属于电解质,其他化合物都是非电解质 |
| C、电解质在通电时发生电离 |
| D、电解质与非电解质的本质区别是在一定条件下能否电离 |
下列关于金属保护的说法不正确的是( )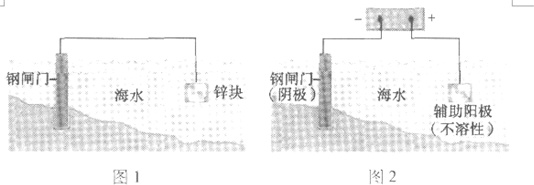

| A、图1是牺牲阳极阴极保护法,图2是外加电流阴极保护法 |
| B、两种保护法共同点是被保护的钢闸门上均为电子流出 |
| C、图1中的负极反应是Zn-2e-═Zn2+ |
| D、图2中钢闸门表面发生还原反应 |
浓硫酸、新制氯水、浓盐酸分别滴在蓝色石蕊试纸上,最终试纸的颜色分别是( )
| A、黑色、红色、红色 |
| B、红色、红色、红色 |
| C、黑色、白色、红色 |
| D、红色、白色、黑色 |
下列图示与对应的叙述相符的是( )
A、 如图表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂 |
B、 如图表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A |
C、 如图表示纯碱溶液受热时氢氧根浓度随温度的变化 |
D、 如图是用0.100 0 mol?L-1的盐酸滴定20.00 mL Na2CO3溶液的曲线,从a→b点反应得离子方程式为HCO3-+H+═CO2↑+H2O |
下列操作中错误的是.( )
| A、除去乙酸乙酯中的少量乙酸:加入乙醇和浓硫酸,使乙酸全部转化为乙酸乙酯 |
| B、分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃):蒸馏 |
| C、取待测液与氢氧化钠共热,产生刺激性气体能使湿润的红色石蕊试纸变蓝,含NH4+ |
| D、分离溶解在水中的少量溴:加入CCl4,使用分液漏斗进行萃取 |