题目内容
水溶液中存在多种平衡,请回答下列问题.
(1)有下列几种溶液:a.NH3?H2O b.CH3COONa c.NH4Cl d.NaHSO4
常温下呈酸性的溶液有 (填序号).
(2)已知25C° 时,醋酸的Ka=1.8×10-5 碳酸的Ka1=4.3×10-7 Ka2=5.6×10-11.有①NaHCO3溶液②CH3COONa溶液③NaOH溶液各25mL,浓度均为0.1mol?L-1三种溶液的pH由大到小顺序为 (请用序号填空);已知NaHCO3溶液呈碱性,该溶液中除水的电离外还存在着两个平衡,用电离方程式或离子方程式表示: 、 ,该溶液中的离子浓度由大到小的顺序是:
(3)有浓度均为0.1mol?L-1的 ①盐酸 ②硫酸 ③醋酸三种溶液,(请用序号填空) 三种溶液的pH由大到小的顺序为 ;中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次的大小关系为 ;
(4)25℃时,AgCl的Ksp=1.8×10-10,试写出AgCl溶解平衡的表达式: ,现将足量AgCl固体投入100mL0.1mol/L MgCl2溶液充分搅拌后冷却到25℃时,此时c(Ag+)= mol/L(忽略溶液体积的变化).
(1)有下列几种溶液:a.NH3?H2O b.CH3COONa c.NH4Cl d.NaHSO4
常温下呈酸性的溶液有
(2)已知25C° 时,醋酸的Ka=1.8×10-5 碳酸的Ka1=4.3×10-7 Ka2=5.6×10-11.有①NaHCO3溶液②CH3COONa溶液③NaOH溶液各25mL,浓度均为0.1mol?L-1三种溶液的pH由大到小顺序为
(3)有浓度均为0.1mol?L-1的 ①盐酸 ②硫酸 ③醋酸三种溶液,(请用序号填空) 三种溶液的pH由大到小的顺序为
(4)25℃时,AgCl的Ksp=1.8×10-10,试写出AgCl溶解平衡的表达式:
考点:弱电解质在水溶液中的电离平衡,盐类水解的应用,难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:(1)弱酸根离子水解显酸性,电离出氢离子的物质其水溶液显酸性;
(2)Ka越大,酸性越强,其对应盐的水解越小;NaHCO3溶液中HCO3-存在电离平衡和水解平衡,HCO3-水解程度大于电离程度而使溶液呈碱性,溶液呈存在电荷守恒,无论电离程度还是水解程度都较小;
(3)氢离子浓度越大,酸性越强,其pH越小.氢离子浓度越小,消耗的碱的量越少;
(4)氯化银的溶解平衡的表达式AgCl(S)?Ag+(aq)+Cl-(aq),c(Ag+)=
.
(2)Ka越大,酸性越强,其对应盐的水解越小;NaHCO3溶液中HCO3-存在电离平衡和水解平衡,HCO3-水解程度大于电离程度而使溶液呈碱性,溶液呈存在电荷守恒,无论电离程度还是水解程度都较小;
(3)氢离子浓度越大,酸性越强,其pH越小.氢离子浓度越小,消耗的碱的量越少;
(4)氯化银的溶解平衡的表达式AgCl(S)?Ag+(aq)+Cl-(aq),c(Ag+)=
| Ksp |
| c(Cl-) |
解答:
解:(1)强酸酸式盐、强酸弱碱盐、酸溶液都呈酸性,NH4Cl为强酸弱碱盐,铵根离子水解而使溶液呈酸性,NaHSO4完全电离出氢离子而使溶液呈强酸性,所以呈酸性的溶液是氯化铵和硫酸氢钠,故答案为:cd;
(2)Ka越大,酸性越强,其对应盐的水解越小,则浓度均为0.1mol?L-1三种溶液,pH最大的为NaOH,醋酸酸性大于碳酸,则碳酸氢钠水解大,碱性强,所以pH由大到小顺序为③①②;
NaHCO3溶液中HCO3-存在电离平衡和水解平衡,方程式分别为:HCO3-?H++CO32-、HCO3-+H2O?H2CO3+OH-;钠离子不水解,碳酸氢根离子水解,所以c(Na+)>c(HCO3-),碳酸氢钠水解而使溶液呈碱性,所以c(OH-)>c(H+),但水解是微弱的,溶液中阴离子主要以碳酸氢根离子存在,所以c(HCO3-)>c(OH-),溶液中碳酸氢根离子电离出氢离子和碳酸根离子、水电离出氢离子,所以c(H+)>c(CO32-),故溶液中各种离子浓度大小顺序是c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-);
故答案为:③①②;HCO3-?H++CO32-;HCO3-+H2O?H2CO3+OH-;c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-);
(3)硫酸为二元强酸,盐酸为以元强酸,醋酸为一远弱酸,等浓度时硫酸中氢离子浓度最大,醋酸中氢离子浓度最小,则三种溶液的pH值由大到小的顺序为③①②,氢离子浓度越小,消耗的碱的量越少,即氢离子浓度越小,中和一定量NaOH溶液生成正盐时,消耗的酸的体积越大,所以消耗三种酸的体积依次的大小关系为②③①,
故答案为:③①②;②③①;
(4)氯化银的溶解平衡的表达式AgCl(S)?Ag+(aq)+Cl-(aq),c(Ag+)=
=
mol/L=9×10-10mol/L,
故答案为:AgCl(S)?Ag+(aq)+Cl-(aq);9×10-10.
(2)Ka越大,酸性越强,其对应盐的水解越小,则浓度均为0.1mol?L-1三种溶液,pH最大的为NaOH,醋酸酸性大于碳酸,则碳酸氢钠水解大,碱性强,所以pH由大到小顺序为③①②;
NaHCO3溶液中HCO3-存在电离平衡和水解平衡,方程式分别为:HCO3-?H++CO32-、HCO3-+H2O?H2CO3+OH-;钠离子不水解,碳酸氢根离子水解,所以c(Na+)>c(HCO3-),碳酸氢钠水解而使溶液呈碱性,所以c(OH-)>c(H+),但水解是微弱的,溶液中阴离子主要以碳酸氢根离子存在,所以c(HCO3-)>c(OH-),溶液中碳酸氢根离子电离出氢离子和碳酸根离子、水电离出氢离子,所以c(H+)>c(CO32-),故溶液中各种离子浓度大小顺序是c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-);
故答案为:③①②;HCO3-?H++CO32-;HCO3-+H2O?H2CO3+OH-;c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-);
(3)硫酸为二元强酸,盐酸为以元强酸,醋酸为一远弱酸,等浓度时硫酸中氢离子浓度最大,醋酸中氢离子浓度最小,则三种溶液的pH值由大到小的顺序为③①②,氢离子浓度越小,消耗的碱的量越少,即氢离子浓度越小,中和一定量NaOH溶液生成正盐时,消耗的酸的体积越大,所以消耗三种酸的体积依次的大小关系为②③①,
故答案为:③①②;②③①;
(4)氯化银的溶解平衡的表达式AgCl(S)?Ag+(aq)+Cl-(aq),c(Ag+)=
| Ksp |
| c(Cl-) |
| 1.8×10-10 |
| 0.2 |
故答案为:AgCl(S)?Ag+(aq)+Cl-(aq);9×10-10.
点评:本题考查了弱电解质的电离、难溶物的溶解平衡、盐类水解等知识点,这些知识点常常综合考查,明确弱电解质的电离程度与弱离子水解程度的关系是解本题关键,再结合溶度积常数分析解答,注意中和一定物质的量的强碱时,需要相同浓度酸的体积与酸的元数有关,与电解质强弱无关,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
关于氧化还原反应的下列说法正确的是( )
| A、含氧酸能起氧化作用,无氧酸则不能 |
| B、阳离子只有氧化性,阴离子只有还原性 |
| C、失电子难的原子获得电子的能力一定强 |
| D、由X变为X2+的反应是氧化反应 |
硫酸铵是农村常用的一种铵态氮肥,试回答下列问题:
某硫酸铵肥料,试验测得氮的质量分数为20%,该样品中可能混有( )
某硫酸铵肥料,试验测得氮的质量分数为20%,该样品中可能混有( )
| A、碳酸氢铵 | B、硝酸铵 |
| C、氯化铵 | D、磷酸氢二铵 |
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.依据溴乙烷的性质,请你进行以下探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.依据溴乙烷的性质,请你进行以下探究.


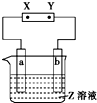
 高炉炼铁中发生的基本反应之一如下:FeO(固)+CO(气)?Fe(固)+CO2(气)(△H>0).
高炉炼铁中发生的基本反应之一如下:FeO(固)+CO(气)?Fe(固)+CO2(气)(△H>0).
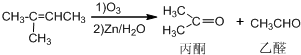
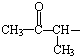 、且属于酯类的同分异构体:
、且属于酯类的同分异构体:
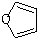 )也可以发生“Diels-Alder反应”,该化学反应方程式为:
)也可以发生“Diels-Alder反应”,该化学反应方程式为: