题目内容
14.请写出醋酸(CH3COOH)与鸡蛋壳(主要成分为CaCO3)反应的离子方程式CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-.分析 醋酸与碳酸钙反应生成醋酸钙、二氧化碳气体和水,其中醋酸为弱酸,碳酸钙为难溶物,二者在离子方程式中都需要保留化学式,据此写出反应的离子方程式.
解答 解:醋酸为弱电解质,离子方程式中需要保留分子式,碳酸钙为难溶物,也不能拆开,二者反应生成醋酸钙、二氧化碳气体和水,反应的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,
故答案为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-.
点评 本题考查了离子方程式的书写,题目难度不大,明确离子方程式的书写原则为解答关键,注意常见的难溶物、弱电解质,试题培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.如图表示298K时N2与H2反应过程中的能量变化.根据如图叙述正确的是( )


| A. | 该反应的热化学方程式为$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g)△H=-92kJ•mol-1 | |
| B. | 不用催化剂,生成1molNH3放出的热量为46kJ,加入催化剂,生成1molNH3放出的热量为小于46kJ | |
| C. | 加入催化剂,降低了正反应的活化能,升高了逆反应的活化能 | |
| D. | 在温度、体积一定的条件下,通入1molN2和3molH2,反应后放出的热量为Q1,若通入2molN2和6molH2,反应后放出的热量为Q2,则Q1<0.5Q2<92KJ |
11.已知10HNO3(稀)+4Zn=4Zn(NO3)2+a+5H2O,若a为氮的氧化物,则a为( )
| A. | NO | B. | NO2 | C. | N2O | D. | N2O3 |
 ;
;
 2SO3.
2SO3. ;
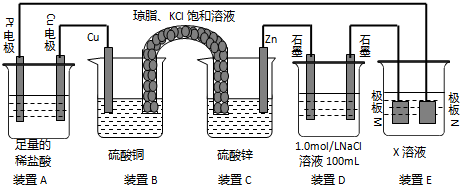
; 请根据下图装置回答
请根据下图装置回答