题目内容
在一定条件下,将m体积NO和n体积O2同时通入倒立于水中且盛满水的容器内,充分反应后,容器内残留m/2体积的气体,该气体与空气接触后变为红棕色,则m与n的比值为( )
A.3:2 B.2:3 C.8:3 D.3:8
【答案】
C
【解析】
试题分析:气体与空气接触后变为红棕色,说明反应后NO是过量的。NO和氧气同时通入水中的化学方程式是4NO+3O2+2H2O=4HNO3,所以参加该反应的NO是 ,所以氧气的体积是
,所以氧气的体积是 ,所以m与n的比值为8:3,答案选C。
,所以m与n的比值为8:3,答案选C。
考点:考查NO和氧气溶于水的有关计算。
点评:该题通过氮的氧化物溶于水的有关计算,训练学生通过化学反应进行的有关计算,特别是在计算过程中的有关讨论的计算。该题属于中等难度的试题。

练习册系列答案
相关题目
 (2013?海淀区二模)一种重要的药物中间体E的结构简式为:
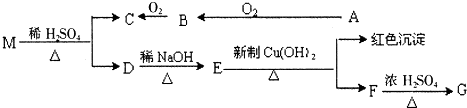
(2013?海淀区二模)一种重要的药物中间体E的结构简式为: ,合成E和高分子树脂N的路线如图所示:
,合成E和高分子树脂N的路线如图所示:


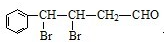 ,下列有关X的说法正确的是
,下列有关X的说法正确的是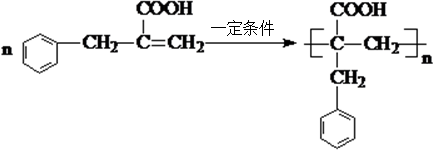


 -OOCCH3
-OOCCH3