题目内容
11.某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见图.下列有关说法错误的是( )
| A. | a极为负极,电极上发生氧化反应 | |
| B. | 电池总反应可表示为:2H2+O2═2H2O | |
| C. | 外电路中电子由b电极通过导线流向a电极 | |
| D. | 该装置工作时把电能转化为化学能 |
分析 通入氢气的一极为电池的负极,发生氧化反应,反应为H2-2e-═2H+,通入氧气的一极为电池的正极,发生还原反应,反应为O2+4e-+4H+=2H2O;电池工作时,电子通过外电路从负极流向正极,由此分析解答.
解答 解:A.因氢元素的化合价升高,则a为负极,负极上氢气失电子发生氧化反应,故A正确;
B.负极反应为H2-2e-═2H+,正极反应为O2+4e-+4H+=2H2O,则电池总反应可表示为:2H2+O2═2H2O,故B正确;
C.电子从负极流向正极,即电子应该是通过外电路由a极流向b,故C错误;
D.该装置为原电池,工作时把化学能转化为电能,故D错误.
故选CD.
点评 本题考查燃料电池的工作原理,学习中要明确电子以及离子的定向移动问题,要能正确判断原电池的正负极,以及电极反应式的书写问题,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.在烷烃分子中,每增加一个碳原子,每摩尔该烷烃完全燃烧需要多消耗氧气( )
| A. | 1 mol | B. | 1.5 mol | C. | 2 mol | D. | 2.5 mol |
2.将盛有20mL NO和NO2混合气体的量筒倒立于水槽中,反应后气体体积缩小为15mL,则原混合气体中NO和NO2的体积比是( )
| A. | 4:1 | B. | 3:2 | C. | 5:3 | D. | 1:4 |
19.将CH3COOH和H18OC2H5在一定条件下发生酯化反应,已知酯化反应是可逆的,反应达到平衡后下列说法正确的是( )
| A. | 18O存在于所有物质中 | B. | 有的乙醇分子可能不含18O | ||
| C. | 所得酯的相对分子质量为88 | D. | 18O仅存在于乙醇和乙酸乙酯里 |
6.下列实验操作中正确的是( )
| A. |  向试管中滴加液体 | B. |  检查装置的气密性 | ||
| C. |  移走加热的蒸发皿 | D. |  加热液体 |
16.已知某溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组成( )
| A. | CH3COO- | B. | NH4+ | C. | Fe2+ | D. | Ba2+ |
3.下列属于强电解质的是( )
| A. | NaCl溶液 | B. | HClO | C. | NaOH | D. | 蔗糖 |
20. 根据以下背景资料,回答下列问题:
根据以下背景资料,回答下列问题:
Ⅰ、不锈钢以其优异的抗腐蚀性能越来越受到人们的靑睐,它主要是由铁、铬、镍、铜、碳等元索所组成的合金.
Ⅱ、锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛.
Ⅲ、K2Cr2O7曾用于检测司机是否酒后驾驶:
Cr2O72-(橙色)+CH3CH2OH→Cr3+(绿色)+CH3COOH (未配平)
(1)镍元素基态原子的电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2.
(2)CH3COOH分子中所含元素的电负性由大到小的顺序为O>C>H,碳原子的轨道杂化类型为sp3和sp2,所含σ键与π键的数目之比为7:1.
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因GeCl4、GeBr4、GeI4的熔、沸点依次增高,原因是分子结构相似,分子量依次增大,分子间相互作用力逐渐增强.
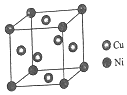
(4)某镍白铜合金的立方晶胞结构如图所示.
①晶胞中铜原子与镍原子的数量比为3:1.
②若合金的密度为dg/cm3,晶胞参数a=$\root{3}{\frac{251}{d{N}_{A}}}$×107nm.
 根据以下背景资料,回答下列问题:
根据以下背景资料,回答下列问题:Ⅰ、不锈钢以其优异的抗腐蚀性能越来越受到人们的靑睐,它主要是由铁、铬、镍、铜、碳等元索所组成的合金.
Ⅱ、锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛.
Ⅲ、K2Cr2O7曾用于检测司机是否酒后驾驶:
Cr2O72-(橙色)+CH3CH2OH→Cr3+(绿色)+CH3COOH (未配平)
(1)镍元素基态原子的电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2.
(2)CH3COOH分子中所含元素的电负性由大到小的顺序为O>C>H,碳原子的轨道杂化类型为sp3和sp2,所含σ键与π键的数目之比为7:1.
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因GeCl4、GeBr4、GeI4的熔、沸点依次增高,原因是分子结构相似,分子量依次增大,分子间相互作用力逐渐增强.
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
①晶胞中铜原子与镍原子的数量比为3:1.
②若合金的密度为dg/cm3,晶胞参数a=$\root{3}{\frac{251}{d{N}_{A}}}$×107nm.