题目内容
1mol CO2和2mol H2的混合气体加热到一定的温度时,可建立下列平衡:CO2+H2?CO+H2O,此时生成的CO的物质的量是0.6mol,若在相同条件下将H2改为4mol,反应达到平衡时,生成的CO的物质的量可能为( )
分析:在相同条件下将H2的物质的量由2mol改为4mol,氢气的浓度增大,平衡向正反应移动,新平衡时CO的物质的量增大,增大氢气的浓度,氢气的转化率降低,计算原平衡氢气的转化率,假定氢气的转化率不变,计算参加反应的氢气物质的量,结合CO2的物质的量为1mol,根据过量计算判断新平衡时CO物质的量的极大值,据此判断.
解答:解:在相同条件下将H2的物质的量由2mol改为4mol,氢气的浓度增大,平衡向正反应移动,新平衡时CO的物质的量增大,即大于0.6mol,
由方程式可知生成0.6molCO需要氢气的物质的量为0.6mol,故氢气的转化率为
×100%=30%,在相同条件下将H2改为4mol,假定氢气的转化率不变,则参加反应的氢气为4mol×30%=1.2mol,需要二氧化碳1.2mol,故根据二氧化碳计算生成CO的极大值,二氧化碳完全反应为极大值,故CO的极大值为1mol,增大氢气的浓度,氢气的转化率降低,故新平衡时0.6mol<n(CO)<1mol,故选C.
由方程式可知生成0.6molCO需要氢气的物质的量为0.6mol,故氢气的转化率为
| 0.6mol |
| 2mol |
点评:考查化学平衡的有关计算、影响化学平衡因素,难度中等,注意利用极限假设法判断时,氢气与二氧化碳的过量计算.

练习册系列答案
相关题目
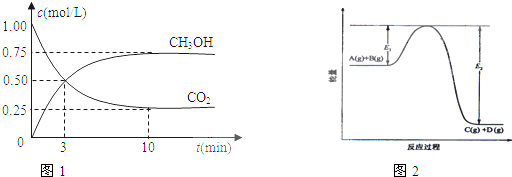
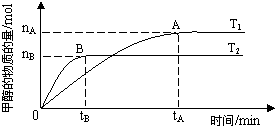 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.