题目内容
9.化学与社会经济建设、生态文明建设、人类健康保障等密切相关.(1)材料是经济和生态文明建设的重要物质基础.
①生产硅酸盐水泥和普通玻璃都需用到的共同原料是石灰石.
②橡胶是制造轮胎的重要原料,橡胶属于C(填字母).
A.金属材料 B.无机非金属材料 C.有机高分子材料
③钢铁制品在潮湿的空气中能发生电化学腐蚀.发生该腐蚀时的负极反应式为Fe-2e-=Fe2+.
(2)防治环境污染,改善生态环境已成为全球共识.
①2013年,全国多个省市出现严重的雾霾天气.导致雾霾形成的主要污染物是C (填字母);
A.O2 B.CO2 C.PM2.5
②采用焚烧处理垃圾进行发电已在江苏投入使用.下列是生活中的常见垃圾.
A.废电池 B.易拉罐 C.玻璃瓶
在焚烧处理前,除废电池外,还有B、C(填字母)应剔除并回收,随意丢弃电池造成的主要危害是重金属污染.
③漂白粉可用于生活用水的杀菌消毒,工业上利用氯气和石灰乳制取漂白粉的化学反应方程式是2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(3)保证食品安全、保持营养均衡,是保障人体健康的基础.
①维生素C能促进人体生长发育.下列富含维生素C的是B(填字母).
A.牛肉 B.辣椒 C.鸡蛋
②缺乏某种微量元素将导致甲状腺肿大,且造成智力损害,该微量元素是A
A.碘 B.铁 C.钙
③人体内蛋白质在蛋白酶作用下,水解为氨基酸,在鸡蛋清溶液中加入饱和硫酸铵溶液有沉淀析出的过程称为盐析.
④使用青霉素可能会产生过敏,在用药前患者一定要进行皮试.
分析 1)①水泥的原料是粘土和石灰石,玻璃的原料是纯碱、石灰石和石英,所以原料中均有石灰石;
②橡胶有天然的和人工合成的,都是高分子材料;
③钢铁是铁的合金易发生电化学腐蚀;Fe失电子作负极;
(2)①PM2.5”是指大气层中直径≥2.5μm的颗粒物,能被肺吸收并进入血液,对人体危害很大,是形成雾霾的主要污染物;
②不能燃烧的垃圾,不能采用焚烧处理;
③氯气和石灰乳反应生成氯化钙、次氯酸钙、水;
(3)①蔬菜中富含维生素C;
②碘元素被称为智力元素;
③蛋白质水解生成氨基酸,蛋白质能发生盐析;
④部分抗生素会产生不良反应要做皮试.
解答 解:(1)①生产玻璃的原料是纯碱、石灰石和石英,高温下,碳酸钠、碳酸钙和二氧化硅反应分别生成硅酸钠、硅酸钙;
生产水泥以黏土和石灰石为主要原料,经研磨、混合后在水泥回转窑中煅烧,再加入适量石膏,并研成细粉就得到普通水泥;所以在玻璃工业、水泥工业中都用到的原料是石灰石,
故答案为:石灰石(或CaCO3);
②橡胶分为天然橡胶和合成橡胶,天然橡胶的成分是聚异戊二烯 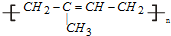 ,合成橡胶主要指:顺丁橡胶、氯丁橡胶、丁苯橡胶等,都为有机高分子材料,
,合成橡胶主要指:顺丁橡胶、氯丁橡胶、丁苯橡胶等,都为有机高分子材料,
故答案为:C;
③钢铁是铁的合金在潮湿的空气中易发生电化学腐蚀;Fe失电子作负极,Fe失去电子生成二价铁离子,其电极反应为:Fe-2e-=Fe2+;
故答案为:电化学;Fe-2e-=Fe2+;
(2)①导致雾霾形成的主要污染物是pM2.5,能被肺吸收并进入血液,对人体危害很大,故选C;
②易拉罐、玻璃瓶不能燃烧,所以不能采用焚烧处理,电池中的重金属能污染环境,所以不能随意丢弃电池;
故答案为:BC;重金属污染;
③氯气和石灰乳反应生成氯化钙、次氯酸钙、水,该反应为2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;
(3)①蔬菜中富含维生素C,所以富含维生素C的是辣椒,故答案为:B;
②碘元素被称为智力元素,缺乏碘元素将导致甲状腺肿大,且造成智力损害,故答案为:A;
③蛋白质在一定条件下水解生成氨基酸,在蛋白质溶液中加入饱和硫酸铵溶液能发生盐析,即有白色沉淀析出,故答案为:氨基酸;盐析;
④部分抗生素会产生不良反应要做皮试,所以使用青霉素前使用者一定要进行皮肤敏感试验,故答案为:皮试.
点评 本题考查常见的环境污染物、漂白粉的制备和药物的主要成分和疗效等,难度不大,注意知识的积累,本题注重化学与生活的联系,明确化学服务于生活,学会利用化学知识解决生活中的问题.

 名校课堂系列答案
名校课堂系列答案| A. | 1 mol氧气的质量为32 g | |
| B. | 常温常压下,1 mol CO2气体体积约为22.4 L | |
| C. | CO2的摩尔质量为44 g•mol-1 | |
| D. | 1 L 2 mol•L-1的BaCl2溶液中含Cl-的个数为2.408×1024 |
| A. | 1.02 | B. | 1.68 | C. | 1.00 | D. | 0.986 |
4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A. | 若单位时间内生成xmolNO的同时消耗x molNH3,则反应达到平衡状态 | |
| B. | 当混合气体的压强不再改变,则说明反应已达到平衡状态 | |
| C. | 当混合气体的密度不再改变,则说明反应已达到平衡状态 | |
| D. | 达到化学平衡后,若增大容器容积,正反应速率减小,逆反应速率增大 |
| A. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | B. | nCH2=CH2$\stackrel{一定条件}{→}$ | ||
| C. |  +HNO3$→_{加热}^{浓硫酸}$ +HNO3$→_{加热}^{浓硫酸}$ +H2O +H2O | D. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ |
| A. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| B. | 反应条件是加热的反应不一定是吸热反应 | |
| C. | 放热反应的反应热总是大于吸热反应的反应热 | |
| D. | 化学反应放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量 |
 .
.