题目内容
 密闭容器中进行下列反应:M(g)+N(g)?R(g)+2L,如图所示R%是R的体积分数,t是时间,下列关于该反应的分析正确的是( )
密闭容器中进行下列反应:M(g)+N(g)?R(g)+2L,如图所示R%是R的体积分数,t是时间,下列关于该反应的分析正确的是( )| A、正反应吸热,L为气体 | B、正反应吸热,L为固体或纯液体 | C、正反应放热,L为气体 | D、正反应放热,L为固体或纯液体 |
分析:升高温度,化学平衡向着吸热方向进行,反之向着放热方向进行,增大压强,化学平衡向着气体系数和减小的方向进行,反之向着气体系数和增大的方向进行.
解答:解:根据图示信息知道,压强不变,温度升高,R的百分含量减小,所以化学平衡逆向移动,说明正向是一个放热反应;
温度不变,增大压强,R的百分含量减小,说明平衡逆向移动,则L为气体.
故选C.
温度不变,增大压强,R的百分含量减小,说明平衡逆向移动,则L为气体.
故选C.
点评:本题考查学生影响化学平衡移动的因素:温度、压强,注意控制变量法在解题中的应用,难度不大.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目


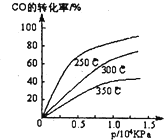 工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH30H(g)
工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH30H(g) 2NO2(g) ΔH=+52.70 kJ·mol—1。
2NO2(g) ΔH=+52.70 kJ·mol—1。
 2NO2(g) ΔH=+52.70 kJ·mol—1。
2NO2(g) ΔH=+52.70 kJ·mol—1。
