题目内容
锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。回答下列问题:
(1)单质铝溶于过量氢氧化钠溶液后,溶液中铝元素的存在形式为 (用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式: 。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是 。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因: 。
(1)单质铝溶于过量氢氧化钠溶液后,溶液中铝元素的存在形式为 (用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式: 。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是 。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因: 。
(1)[Al(OH)4]- (2)Zn+2NaOH+2H2O=Na2[Zn(OH)4]+H2↑ (3)①③④ (4)可溶性锌盐与氨水反应产生的Zn(OH)2可溶于过量氨水中,生成[Zn(NH3)4]2+,氨水的量不易控制
(1)Al与NaOH发生反应:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑。溶液中Al以[Al(OH)4]-形式存在。(2)依照Al和NaOH发生的反应,可以写出Zn与NaOH反应的化学方程式:Zn+2NaOH+2H2O=Na2[Zn(OH)4]+H2↑。(3)①少量Al2(SO4)3滴入NaOH中,没有沉淀生成,生成[Al(OH)4]-,少量NaOH滴入Al2(SO4)3中,有沉淀生成。②Al2(SO4)3滴入氨水中,有沉淀生成;氨水滴入Al2(SO4)3中,也有沉淀生成。③少量ZnSO4滴入NaOH中,没有沉淀生成,生成[Zn(OH)4]2-;少量NaOH滴入ZnSO4中,有沉淀生成。④少量ZnSO4滴入氨水中,没有沉淀生成,生成[Zn(NH3)4]2+;少量氨水滴入ZnSO4中,有沉淀生成。所以用相互滴加的实验方法就能鉴别的有①③④。(4)可溶性锌盐与氨水反应产生的Zn(OH)2可溶于过量氨水,生成[Zn(NH3)4]2+,实验过程中加入氨水的量不易控制。

练习册系列答案
相关题目
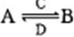 (在水溶液中进行)。其中C是产生温室效应的气体;D是淡黄色固体。写出C的结构式 ;D的电子式
(在水溶液中进行)。其中C是产生温室效应的气体;D是淡黄色固体。写出C的结构式 ;D的电子式 


 2SO3(g) △H1 = -197 kJ /mol;
2SO3(g) △H1 = -197 kJ /mol;