题目内容
(14分)X,Y,Z,Q,R是五种短周期元素,原子序数依次增大。X,Y两元素最高正价与最低负价代数和均为0;Q与X同主族;Z是地壳中含量最高的非金属元素,R的简单离子在同周期离子中半径最小。请回答下列问题:
(1)画出Z的原子结构示意图 ,工业上制取R单质的化学方程式为
(2)已知,由X,Y两种元素组成的相对分子质量最小的化合物W 3.2g在氧气中完全燃烧生成稳定化合物(常温常压下)放出178.06KJ的热量,写出W燃烧的热化学方程式
(3)由以上某些元素组成的化合物A,B,C,D有如下转化关系: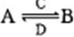 (在水溶液中进行)。其中C是产生温室效应的气体;D是淡黄色固体。写出C的结构式 ;D的电子式
(在水溶液中进行)。其中C是产生温室效应的气体;D是淡黄色固体。写出C的结构式 ;D的电子式
①如果A,B均由三种元素组成,B为两性化合物,且不溶于水,则由A转化为B的离子方程式为
②如果A,B均为由以上某些元素组成的盐,则A溶液显 性,原因是(用离子方程式表示) 。浓度均为0.1mol/L的A,B的溶液等体积混合,混合溶液中离子浓度由大到小的顺序为 。
(1)画出Z的原子结构示意图 ,工业上制取R单质的化学方程式为
(2)已知,由X,Y两种元素组成的相对分子质量最小的化合物W 3.2g在氧气中完全燃烧生成稳定化合物(常温常压下)放出178.06KJ的热量,写出W燃烧的热化学方程式
(3)由以上某些元素组成的化合物A,B,C,D有如下转化关系:
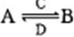 (在水溶液中进行)。其中C是产生温室效应的气体;D是淡黄色固体。写出C的结构式 ;D的电子式
(在水溶液中进行)。其中C是产生温室效应的气体;D是淡黄色固体。写出C的结构式 ;D的电子式 ①如果A,B均由三种元素组成,B为两性化合物,且不溶于水,则由A转化为B的离子方程式为
②如果A,B均为由以上某些元素组成的盐,则A溶液显 性,原因是(用离子方程式表示) 。浓度均为0.1mol/L的A,B的溶液等体积混合,混合溶液中离子浓度由大到小的顺序为 。
(1)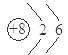 2Al2O3
2Al2O3 4Al+3O2↑
4Al+3O2↑
(2)CH4(g)+2O2(g)=CO2(g)+2H2O(l) ?H=—890.3KJ/mol
(3)O=C=O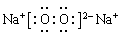
①AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-或2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-
②碱 CO32-+H2O HCO3-+OH- c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
HCO3-+OH- c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
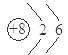 2Al2O3
2Al2O3 4Al+3O2↑
4Al+3O2↑(2)CH4(g)+2O2(g)=CO2(g)+2H2O(l) ?H=—890.3KJ/mol
(3)O=C=O
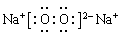
①AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-或2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-
②碱 CO32-+H2O
 HCO3-+OH- c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
HCO3-+OH- c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)试题分析:根据题意可得X是H;Y是C;Z是O;Q是Na;R是Al。(1)8号元素O的原子结构示意图为
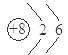 ;Al的活动性比较强,在工业上只能用电解熔融的Al2O3的方法进行冶炼。反应的方程式为
;Al的活动性比较强,在工业上只能用电解熔融的Al2O3的方法进行冶炼。反应的方程式为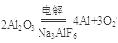 。(2)C、H两元素组成的相对分子质量最小的物质为CH4,3.2g CH4的物质的量为3.2g÷16g/mol=0.2mol.完全燃烧放出178.06KJ的热量。则其燃烧的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l) ?H=—890.3KJ/mol。(3)C是产生温室效应的气体,则C为CO2,其的结构式为O=C=O;D是淡黄色固体则D为Na2O2,其电子式为
。(2)C、H两元素组成的相对分子质量最小的物质为CH4,3.2g CH4的物质的量为3.2g÷16g/mol=0.2mol.完全燃烧放出178.06KJ的热量。则其燃烧的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l) ?H=—890.3KJ/mol。(3)C是产生温室效应的气体,则C为CO2,其的结构式为O=C=O;D是淡黄色固体则D为Na2O2,其电子式为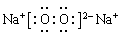 。①如果A,B均由三种元素组成,B为两性化合物,且不溶于水,则A为NaAlO2,B为Al(OH)3.则由A转化为B的离子方程式为AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-或2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-。②如果A,B均为由以上某些元素组成的盐,则A为Na2CO3;B为NaHCO3.Na2CO3是强碱弱酸盐,弱酸根离子CO32-水解CO32-+ H2O
。①如果A,B均由三种元素组成,B为两性化合物,且不溶于水,则A为NaAlO2,B为Al(OH)3.则由A转化为B的离子方程式为AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-或2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-。②如果A,B均为由以上某些元素组成的盐,则A为Na2CO3;B为NaHCO3.Na2CO3是强碱弱酸盐,弱酸根离子CO32-水解CO32-+ H2O HCO3-+OH-。消耗水电离产生的H+,当最终达到平衡时,使溶液中的OH-的浓度增大,导致溶液显碱性。若将Na2CO3和NaHCO3等浓度等体积混合,则由于CO32-水解、HCO3-都发生水解反应,所以溶液显碱性,c(OH-)>c(H+);水解程度 CO32->HCO3-,所以c(HCO3-)>c(CO32-)。盐的水解程度是很微弱的,盐的电离作用远大于盐的水解作用,所以c(CO32-)>c(OH-);因为Na+由Na2CO3和NaHCO3共同电离产生,所以c(Na+)>c(HCO3-)。故离子浓度的大小关系为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)。
HCO3-+OH-。消耗水电离产生的H+,当最终达到平衡时,使溶液中的OH-的浓度增大,导致溶液显碱性。若将Na2CO3和NaHCO3等浓度等体积混合,则由于CO32-水解、HCO3-都发生水解反应,所以溶液显碱性,c(OH-)>c(H+);水解程度 CO32->HCO3-,所以c(HCO3-)>c(CO32-)。盐的水解程度是很微弱的,盐的电离作用远大于盐的水解作用,所以c(CO32-)>c(OH-);因为Na+由Na2CO3和NaHCO3共同电离产生,所以c(Na+)>c(HCO3-)。故离子浓度的大小关系为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)。
练习册系列答案
相关题目