题目内容
铝的阳极氧化是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸。
某化学研究小组在实验室中按下列步骤模拟铝表面“钝化”的产生过程。
(1)配制实验用的溶液。要配制200 mL密度为1.2 g/cm3的溶质质量分数为16%的NaOH溶液,需要称取________g NaOH固体。
(2)把铝片浸入热的16%的NaOH溶液中约半分钟左右洗去油污,除去表面的氧化膜,取出用水冲洗,写出除去氧化膜的离子方程式:________。
(3)按下图组装好仪器,接通开关K,通电约25 min。在阳极生成氧化铝,阴极产生气体。
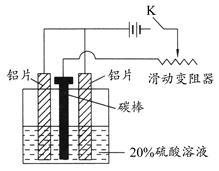
写出该过程中的电极反应式:
阳极:_________________________________________;
阴极:_________________________________________。
(4)断开电路,取出铝片,用质量分数为1%的稀氨水中和表面的酸液,再用水冲洗干净。写出该过程发生反应的离子方程式:______________________。
某化学研究小组在实验室中按下列步骤模拟铝表面“钝化”的产生过程。
(1)配制实验用的溶液。要配制200 mL密度为1.2 g/cm3的溶质质量分数为16%的NaOH溶液,需要称取________g NaOH固体。
(2)把铝片浸入热的16%的NaOH溶液中约半分钟左右洗去油污,除去表面的氧化膜,取出用水冲洗,写出除去氧化膜的离子方程式:________。
(3)按下图组装好仪器,接通开关K,通电约25 min。在阳极生成氧化铝,阴极产生气体。

写出该过程中的电极反应式:
阳极:_________________________________________;
阴极:_________________________________________。
(4)断开电路,取出铝片,用质量分数为1%的稀氨水中和表面的酸液,再用水冲洗干净。写出该过程发生反应的离子方程式:______________________。
(1)38.4 (2)Al2O3+2OH-+3H2O=2[Al(OH)4]- (3)2Al+3H2O-6e-=Al2O3+6H+;6H++6e-=3H2↑ (4)NH3·H2O+H+=NH4++H2O
(1)m[NaOH(aq)]=ρV=200 mL×1.2 g/cm3=240 g,m(NaOH)=m[NaOH(aq)]·w(NaOH)=240 g×16%=38.4 g。(2)铝片表面的氧化膜为Al2O3,是一种两性氧化物,可与强碱反应生成偏铝酸盐和水。(3)阳极是Al失去电子,与H2O共同作用转化成Al2O3;阴极是电解质溶液中的H+得到电子而转化成H2。(4)NH3·H2O属于弱碱,写离子方程式时要写成化学式的形式。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目