题目内容
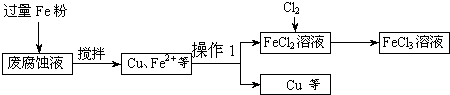
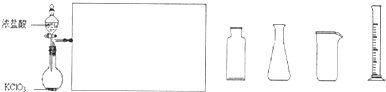
14.2g Cl2 含 个氯气分子、 摩尔氯原子,标准状况下所占的体积为 升,与这些Cl2分子数相同的H2的质量是 g ,它们恰好完全反应后得到的氯化氢气体的物质的量是 摩尔,质量为 g,在标准状况下是 升,将产生的氯化氢气体溶于490.4 mL 水中,则所得溶液的质量为 g ,若所得溶液的密度为1.01 g?cm-3 ,则该溶液的体积为 L。 溶液的物质的量浓度为 mol?L-1 ,质量分数为 。
0.2NA或1.204×1023 ,0.4 , 4.48 ,0.4 , 0.4 ,14.6 , 8.96 , 505 , 0.8 ,2.89%或0.0289

练习册系列答案
相关题目