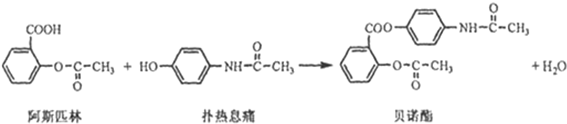
题目内容
下列叙述正确的是
- A.不填将浓硫酸沾在皮肤上,立即用NaOH溶液冲洗
- B.将浓硝酸保存在棕色细口玻璃瓶中
- C.制备乙酸乙酯时,将乙醇和乙酸依次加入浓硫酸中
- D.为检验酸性溶液中是否含有Cl-和SO42-,先加入硝酸银溶液,滤去沉淀后再加入硝酸钡溶液
B
分析:A.NaOH溶液有腐蚀性;
B.浓硝酸见光易分解;
C.将密度大的浓硫酸加入到密度小的溶液,防止液体飞溅,冷却后加乙酸防止过热乙酸挥发;
D.白色不溶于硝酸的沉淀有氯化银和硫酸钡.
解答:A.浓硫酸溶于水并放热,且具有强腐蚀性,少量浓硫酸沾在皮肤上,应先用干抹布拭去,再用大量的水冲洗,最后涂上碳酸氢钠溶液,故A错误;
B.浓硝酸见光易分解,必须保存在棕色的细口瓶中,故B正确;
C.乙醇、乙酸和浓硫酸的混合液的方法是:先加入乙醇,然后沿着试管壁慢慢加入浓硫酸,冷却后再加乙酸,故C错误;
D.若溶液中含有亚硫酸根离子,则易被氧化为硫酸根,不能确定是否存在硫酸根,即亚硫酸根离子会干扰,故D错误.
故选B.
点评:本题考查化学实验基本操作,题目难度不大,注意离子的性质以及比较方案的合理性.
分析:A.NaOH溶液有腐蚀性;
B.浓硝酸见光易分解;
C.将密度大的浓硫酸加入到密度小的溶液,防止液体飞溅,冷却后加乙酸防止过热乙酸挥发;
D.白色不溶于硝酸的沉淀有氯化银和硫酸钡.
解答:A.浓硫酸溶于水并放热,且具有强腐蚀性,少量浓硫酸沾在皮肤上,应先用干抹布拭去,再用大量的水冲洗,最后涂上碳酸氢钠溶液,故A错误;
B.浓硝酸见光易分解,必须保存在棕色的细口瓶中,故B正确;
C.乙醇、乙酸和浓硫酸的混合液的方法是:先加入乙醇,然后沿着试管壁慢慢加入浓硫酸,冷却后再加乙酸,故C错误;
D.若溶液中含有亚硫酸根离子,则易被氧化为硫酸根,不能确定是否存在硫酸根,即亚硫酸根离子会干扰,故D错误.
故选B.
点评:本题考查化学实验基本操作,题目难度不大,注意离子的性质以及比较方案的合理性.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
 (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
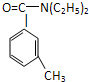 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH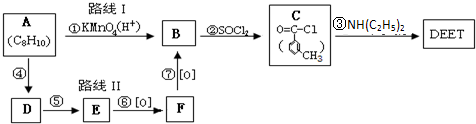
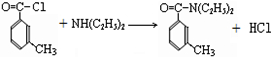
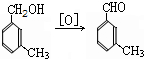
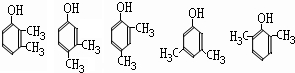 (任写2种)
(任写2种)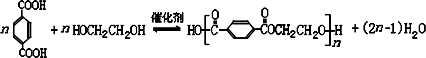
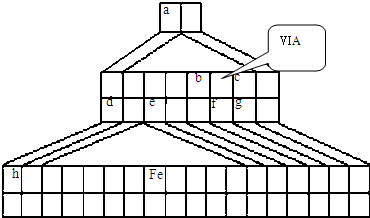
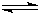 NH3?H2O+H+
NH3?H2O+H+