题目内容
4.30mL浓度为0.05mol/L的Na2SO3溶液恰好与25mL浓度为0.02mol/L的K2R2O7溶液反应,则元素R在还原产物中的化合价是+3.分析 Na2SO3被氧化为Na2SO4,S元素化合价由+4价升高为+6价;K2R2O7中R元素发生还原反应,令R元素在产物中的化合价为a价,根据电子转移守恒计算a的值.
解答 解:令R元素在产物中的化合价为a价,根据电子转移守恒,则:
30×10-3L×0.05mol/L×(6-4)=25×10-3L×0.02mol/L×2×(6-a)
解得a=+3
故答案为:+3.
点评 本题考查氧化还原反应计算、氧化还原反应概念等,难度不大,表示出得失数目是解题关键,熟练掌握电子转移守恒思想的运用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列说法正确的是( )
| A. | 取少许某溶液,滴加数滴KSCN溶液,无明显现象;再另取少许原溶液,先滴少量新制氯水,再滴加数滴KSCN溶液,溶液变血红色,则原溶液中一定含Fe2+ | |
| B. | 焰色反应时,用稀硫酸洗净铂丝,并在火焰上灼烧至无色,然后蘸取溶液 | |
| C. | 在淀粉溶液中加入稀硫酸并加热片刻后,再加入适量银氨溶液,水浴加热后没有银镜生成,说明淀粉没有水解 | |
| D. | 测定某溶液的pH,常用干燥洁净的玻璃棒蘸取该溶液滴在润湿的pH试纸上 |
15.下列叙述中正确的是( )
| A. | 甲苯分子中共平面的原子最多是12个 | |
| B. | 对二甲苯分子中有4个碳原子在一条直线上 | |
| C. | 1-丁烯分子中的4个碳原子一定不在同一平面内 | |
| D. | 2-丁烯分子中的4个碳原子一定不在同一平面内 |
12.用铁片与稀硫酸反应制氢气时,下列措施不能使氢气生成速率加大的是( )
| A. | 加热 | B. | 不用稀硫酸,改用98%浓硫酸 | ||
| C. | 加入硫酸铜 | D. | 不用铁片,改用铁粉 |
19.实验室制备下列气体时,所用方法正确的是( )
| A. | 制氧气时,用Na2O2或H2O2做反应物可选择相同的气体发生装置 | |
| B. | 制氯气时,用饱和NaHCO3和浓硫酸净化气体 | |
| C. | 制氨气时,用排水法或向上排空气法收集气体 | |
| D. | 制二氧化氮时,用水或NaOH溶液吸收尾气 |
16.在一定条件下,对于A2(g)+3B2(g)?2AB3(g)反应来说,下列所表示的化学反应速率中最大的是( )
| A. | v(A2)=0.8 mol•L-1•s-1 | B. | v(A2)=40 mol•L-1•min-1 | ||
| C. | v(AB3)=1.0 mol•L-1•s-1 | D. | v(B2)=1.2 mol•L-1•s-1 |
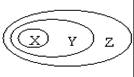 表中所示物质或概念间的从属关系符合右图的是( )
表中所示物质或概念间的从属关系符合右图的是( )