题目内容
3.下列说法正确的是( )| A. | 在由水电离产生的氢离子浓度为10-13 mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3-四种离子能大量共存 | |
| B. | 已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 | |
| C. | 对于反应2N2H4(l)=N2(g)+2H2(g),△H=-50.6 kJ?mol-1,它只在高温下自发进行 | |
| D. | 常温下,将0.2 mol?L-1某一元碱(ROH)溶液和0.1 mol?L-1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+) |
分析 A、在由水电离产生的氢离子浓度为10-13 mol•L-1的溶液可能是酸溶液也可能是碱溶液;
B、MgCO3溶液中,Mg2+离子和CO32-离子都能水解,水解后离子浓度不相等,存在碳酸镁固体的溶液是饱和溶液,所以在相同的温度下,溶度积常数相同;
C、反应2N2H4(l)=N2(g)+2H2(g)△H=-50.6 kJ/mol,为熵增、焓减的反应,常温下也能进行;
D、将0.2 mol•L-1某一元碱ROH溶液和0.1 mol•L-1HCl溶液等体积混合,得到RCl和ROH的混合溶液,混合后溶液pH<7,则水解大于电离.
解答 解:A、在由水电离产生的氢离子浓度为10-13 mol•L-1的溶液可能是酸溶液也可能是碱溶液,所以溶液中不可能大量存在碳酸氢根离子,故A错误;
B、含有固体MgCO3的溶液中,是饱和溶液,Mg2+离子和CO32-离子都能水解,水解后离子浓度可能不相等,但在相同的温度下,溶度积常数不变,故B错误;
C、反应2N2H4(l)=N2(g)+2H2(g)△H=-50.6 kJ/mol,为熵增、焓减的反应,由△G=△H-T△S可知常温下也能进行,故C错误;
D、将0.2 mol•L-1某一元碱ROH溶液和0.1 mol•L-1HCl溶液等体积混合,得到等量的RCl和ROH的混合溶液,混合后溶液pH<7,则水解大于电离,所以c(ROH)>c(R+),故D正确;
故选D.
点评 本题考查离子的共存,明确习题中的信息是解答本题的关键,题目综合性较强,熟悉离子共存,酸碱反应后水解与电离、反应进行的方向、溶度积等知识即可解答,题目难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
19.下列关于F、Cl、Br、I相关物质性质的比较中,不正确的是( )
| A. | 单质的颜色随核电荷数的增加而加深 | |
| B. | 单质的熔、沸点随核电荷数的增加而升高 | |
| C. | 它们的氢化物的还原性随核电荷数的增加而增强 | |
| D. | 它们的氢化物的稳定性随核电荷数的增加而增强 |
11.运用元素周期律分析,下列说法正确的是( )
| A. | 元素的化学性质随着相对原子质量的递增而呈周期性变化 | |
| B. | 元素的最外层电子数等于元素的最高化合价 | |
| C. | 原子序数越大,原子半径越大 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
18.短周期元素X、Y,X元素原子的最外层电子数与次外层电子数的差值等于电子层数;Y元素原子的最外层电子数比X元素原子的最外层电子数多2,则X与Y所形成的化合物的化学式为( )
| A. | X3Y2 | B. | X2Y | C. | X2Y5 | D. | XY3 |
8.用NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 标准状况下,2.24LCHCl3中含有碳氯键数目为0.3NA | |
| B. | 25℃时,0.1mol/L的Na2CO3溶液中含有Na+的数目为0.02NA | |
| C. | 28gN2和CO的混合气体中含有的分子数为NA | |
| D. | 1molNa2O和1molNa2O2的混合物中,含有的离子总数为7NA |
13.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 0.lmol/LCH3COONa溶液:c(Na+)═c(CH3COO-) | |
| B. | 0.1mol/LNa2CO3溶液:c(Na+)═c(HCO3-)+2c(CO32-)+2c(H2CO3) | |
| C. | 向醋酸钠溶液加适量醋酸所得溶液:c(Na+)+c(H+)═c(CH3COO-)+c(OH-) | |
| D. | 常温下,将pH=2的盐酸和pH=12的氨水等体积混合:c(Cl-)>c(NH4+) |
 .
.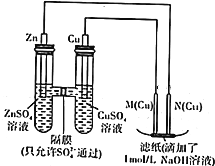 用如图示装置进行实验
用如图示装置进行实验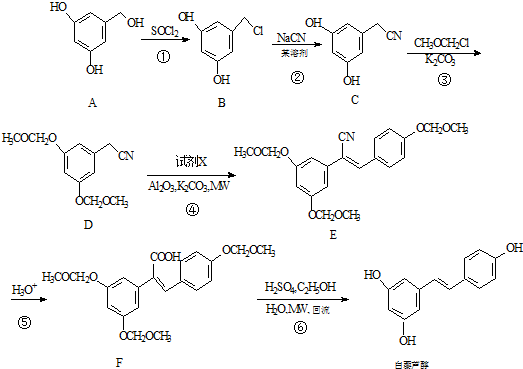
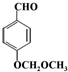 .
.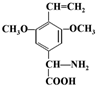 或
或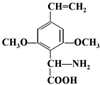 .(任写一种)
.(任写一种)