题目内容
向一定量的Fe、FeO、Fe2O3混合物中加入1.00mol/l的盐酸100ml,可恰好使混合物完全溶解,放出224ml标准状况下的气体,向所得溶液中加入硫氰化钾,无血红色出现。
(1)若用足量的CO在高温下还原相同质量的混合物,能得到铁的质量是多少?
(2)求原混合物中铁元素的质量分数 。
(1)最终溶液为FeCl2
故n(Fe)= n(FeCl2)= 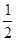 n(Cl-)=
n(Cl-)=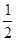 n(HCl)=
n(HCl)=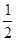 × 1.00mol/L×0.1L=0.05mol
× 1.00mol/L×0.1L=0.05mol
m(Fe)=0.05mol×56g/mol=2.8g
(2)HCl中H元素反应后一部分转化成H2,另一部分转化到H2O中,
故n(O)=n(H2O)=
∴m(O)=0.64g
所以w(Fe)=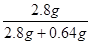 ×%=81.4%
×%=81.4%
解析

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
向一定量的Fe,FeO,Fe2O3,Fe3O4的混合溶液中,加入150mL 4mol/L的稀硝酸,恰好使混合物完全溶解,并放出标准状况下NO气体2.24L,往所得溶液中加KSCN溶液,无红色出现.若用一定量的氢气在加热条件下还原相同质量的该混合物,所得固体的物质的量可能为( )
| A、0.30mol | B、0.28mol | C、0.25mol | D、0.22mol |