题目内容
1.金属单质及其化合物常应用于有机物的反应和分析之中,某芳香族化合物A分子式为C8H10O2 为测定其结构做如下分析:(1)为确定羟基的个数,将1mol A与足量钠反应生成氢气22.4L(标准状况下),说明A分子中含羟基2个.
(2)核磁共振H谱显示A有3个峰,峰面积之比为1:2:2,该物质的结构简式为
 .
.(3)A在Cu催化下可被氧气氧化生成有机物B,B的相对分子质量比A小4.试写出反应的方程式
 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O.
+2H2O.(4)1mol B与足量银氨溶液充分反应生成有机物C,同时得到银432克.将生成的有机物C酸化后得到有机物D.已知A,D在一定条件下可缩聚生成高分子化合物E.
写出E在足量NaOH溶液中水解的化学反应方程式
 +2nNaOH$→_{△}^{NaOH溶液}$n
+2nNaOH$→_{△}^{NaOH溶液}$n +n
+n .
.(5)有机物F是有机物A的一种同分异构体.1mol F与足量钠反应同样生成氢气22.4L(标准状况下),且F能使氯化铁溶液显紫色.试写出满足此条件的有机物F的结构简式
 (或
(或 等)(只写出一种即可).
等)(只写出一种即可).
分析 (1)2mol羟基能够与钠反应生成1mol氢气,据此判断该有机物分子中含有羟基的数目;
(2)核磁共振H谱显示A有3个峰,峰面积之比为1:2:2,芳香族化合物A分子式为C8H10O2,说明A分子具有对称结构,在苯环的对位C上各含有1个-CH2;
(3)醇羟基能够催化氧化生成醛基或羧基,结合B的相对分子质量比A小4可知B为中含有两个醛基;
(4)根据关系式-HCO~2Ag计算出生成银的物质的量及质量;将生成的有机物C( )酸化后得到有机物D,则D为
)酸化后得到有机物D,则D为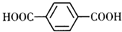 ;已知A,D在一定条件下可缩聚生成高分子化合物E,则E的结构简式为
;已知A,D在一定条件下可缩聚生成高分子化合物E,则E的结构简式为 ,据此写出E在足量NaOH溶液中水解的化学反应方程式;
,据此写出E在足量NaOH溶液中水解的化学反应方程式;
(5)根据A的结构简式、B的性质判断B含有的官能团,然后写出一种满足条件的结构简式.
解答 解:(1)标准状况下22.4L氢气的物质的量为:$\frac{22.4L}{22.4L/mol}$=1mol,生成1mol氢气需要消耗2mol-OH,A分子中含有羟基的数目为:$\frac{2mol}{1mol}$=2,
故答案为:2;
(2)芳香族化合物A分子式为C8H10O2,其不饱和度为:$\frac{8×2+2-10}{2}$=4,1个苯环的不饱和度为4,说明A分子中不含有其它不饱和结构;核磁共振H谱显示A有3个峰,峰面积之比为1:2:2,说明A分子具有对称结构,在苯环的对位C上各含有1个-CH2,则A的结构简式为: ,
,
故答案为: ;
;
(3)A的结构简式为 ,A在Cu催化下可被氧气氧化生成有机物B,B的相对分子质量比A小4,则B分子中含有两个醛基,B的结构简式为:
,A在Cu催化下可被氧气氧化生成有机物B,B的相对分子质量比A小4,则B分子中含有两个醛基,B的结构简式为: ,该反应的化学方程式为:
,该反应的化学方程式为: +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O,
+2H2O,
故答案为: +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O;
+2H2O;
(4)1mol B( )与足量银氨溶液充分反应生成有机物C,则C的结构简式为
)与足量银氨溶液充分反应生成有机物C,则C的结构简式为 ,根据关系式-HCO~2Ag可知,1molB分子中含有2mol醛基,能够置换出4molAg,置换出的银的质量为:108g/mol×4mol=432g;
,根据关系式-HCO~2Ag可知,1molB分子中含有2mol醛基,能够置换出4molAg,置换出的银的质量为:108g/mol×4mol=432g;
将生成的有机物C( )酸化后得到有机物D,则D为
)酸化后得到有机物D,则D为 ;已知A,D在一定条件下可缩聚生成高分子化合物E,则E的结构简式为:
;已知A,D在一定条件下可缩聚生成高分子化合物E,则E的结构简式为: ,则E在足量NaOH溶液中水解的化学反应方程式为:
,则E在足量NaOH溶液中水解的化学反应方程式为: +2nNaOH$→_{△}^{NaOH溶液}$n
+2nNaOH$→_{△}^{NaOH溶液}$n +n
+n ,
,
故答案为:432; +2nNaOH$→_{△}^{NaOH溶液}$n
+2nNaOH$→_{△}^{NaOH溶液}$n +n
+n ;
;
(5)有机物F是有机物A的一种同分异构体,A为 ;1mol F与足量钠反应同样生成氢气22.4L(标准状况下),且F能使氯化铁溶液显紫色,说明F分子中含有2个羟基,至少含有1个酚羟基,则F可能的结构简式如:
;1mol F与足量钠反应同样生成氢气22.4L(标准状况下),且F能使氯化铁溶液显紫色,说明F分子中含有2个羟基,至少含有1个酚羟基,则F可能的结构简式如: 、
、 等,
等,
故答案为: (或
(或 等).
等).
点评 本题考查了有机推断,题目难度中等,明确常见有机物结构与性质为解答关键,注意掌握同分异构体的书写原则,明确常见有机物分子式、结构简式确定方法,试题知识点较多,充分考查了学生的分析能力及灵活应用能力.

 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置及有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是B(填正确选项前的字母)
A.引发反应 B.减少副产物 C.防止乙醇挥发
(2)在装置C中应加入C,其目的是吸收反应中可能生成的酸性气体(填正确选项前的字母)
A.饱和碳酸氢钠溶液 B.浓硫酸 C.氢氧化钠溶液
(3)判断装置D中该制备反应已经结束的最简单方法是观察溴水颜色是否褪尽
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”或“下”)
(5)若产物中有少量副产物乙醚,除去乙醚的方法是蒸馏(填实验操作方法)
| A. | 6个碳原子形成的烃分子中,最多有5个C-C单键 | |
| B. | C2H4的结构简式可表示为CH2CH2 | |
| C. | C3H6分子中一定含有C═C双键 | |
| D. | C6H6分子中,所有原子均可能在同一平面内 |
(1)实验室中通常用NaOH溶液进行洗气和提纯,当用100mL 3mol•L-1的NaOH溶液吸收标准状况下4.48L CO2时,所得溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
(2)常温下,向一定体积的0.1mol•L-1的醋酸溶液中加水稀释后,下列说法正确的是CD.
A.溶液中导电粒子的数目减少 B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中
 不变 D.溶液中
不变 D.溶液中 减小
减小(3)常温下将0.15mol•L-1的稀硫酸V1mL与0.1mol•L-1的NaOH溶液V2mL混合,所得溶液的pH为1,则V1:V2=1:1(溶液体积的变化忽略不计).
(4)常温下,浓度均为0.1mol•L-1的下列五种溶液的pH如表所示:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCNB.HClO C.H2CO3D.CH3COOH
②根据以上数据,判断下列反应可以成立的是AB.
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO D.NaHCO3+HCN=NaCN+H2O+CO2↑
(5)几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |

| A. | 石墨和金刚石的转化是物理变化 | |
| B. | 金刚石的稳定性强于石墨 | |
| C. | 石墨和金刚石是同分异构体 | |
| D. | C(s、石墨)=C(s、金刚石)△H=+1.9 kJ•mol-1 |