��Ŀ����
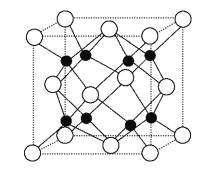
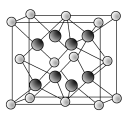
����Ŀ��A��H���ֶ���������Ԫ�������ڱ��е����λ������ͼ��ʾ����֪CԪ���γɵĵ����С�������������������E������������Ӧ��ˮ��������E������⻯�ﷴӦ�������ӻ����
��1��д��B��G��Ӧ��Ԫ�ط���______________ ��
��2��DԪ�������ڱ��е�λ��Ϊ______________��
��3��B��E��F�ļ����Ӱ뾶�ɴ�С��˳��Ϊ______________��д���ӷ��ţ���
��4������Ԫ�����γɵ���̬����������������ˮ��������______________��д��ѧʽ����
��5��B�ĵ�����F�ĵ�����ȼ�յĻ�����ɫΪ______________�����γɻ�����ĵ���ʽΪ______________��
��6��CԪ�صĵ��ʿ�����D��F��ɵ�һ����̬��������ȼ�գ�д���÷�Ӧ�Ļ�ѧ����ʽ________________��
���𰸡� Na��S �ڶ����ڣ����2���ڣ��ڢ�A�� r��N3-) �� r��O2-����r��Na+������N3- ��O2- �� Na+�� Cl2 ��O3 ��ɫ ![]() 2Mg+CO2
2Mg+CO2 ![]() 2MgO+C
2MgO+C
����������֪CԪ���γɵĵ����������������������������C��Mg�������A��H���ֶ���������Ԫ�������ڱ��е����λ�ÿ�֪B��Na��A��Li��E������������Ӧ��ˮ��������E������⻯�ﷴӦ�������ӻ������E��N������D��C��F��O��G��S��H��Cl����
��1���������Ϸ�����֪B��G��Ӧ��Ԫ�ط��ŷֱ���Na��S����2��DԪ����C�������ڱ��е�λ��Ϊ�ڶ����ڵڢ�A�塣��3����������Ų���ͬ�����������뾶��ԭ���������������С����B��E��F�ļ����Ӱ뾶�ɴ�С��˳��Ϊr��N3-) ��r��O2-����r��Na+������4������Ԫ�����γɵ���̬����������������ˮ��������Cl2 ��O3����5��Na������������ȼ�յĻ�����ɫΪ��ɫ�����γɻ������ǹ������ƣ�����ʽΪ![]() ����6��Mg������D��F��ɵ�һ����̬������CO2��ȼ�գ��÷�Ӧ�Ļ�ѧ����ʽΪ2Mg+CO2
����6��Mg������D��F��ɵ�һ����̬������CO2��ȼ�գ��÷�Ӧ�Ļ�ѧ����ʽΪ2Mg+CO2![]() 2MgO+C��
2MgO+C��

 ��ҵ����ϵ�д�
��ҵ����ϵ�д� ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д� �����ܾ�ϵ�д�
�����ܾ�ϵ�д�����Ŀ�����и���ʵ���У���������ֽ�������
H2O2��Ũ�ȣ����������� | �¶ȣ����� | ���� | |
A | 5 | 10 | ��ʹ�� |
B | 5 | 15 | ʹ��FeCl3 |
C | 15 | 20 | ��ʹ�� |
D | 15 | 30 | ʹ��MnO2 |
A. A B. B C. C D. D