题目内容
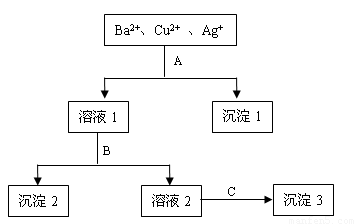
某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离,其流程图如下,请按要求写出最佳答案:
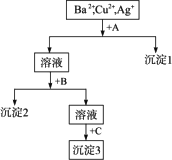
(1)沉淀的化学式:沉淀1________,沉淀2________,沉淀3________.
(2)写出“混合液+A”反应时的离子方程式:________;“溶液+B”反应时的离子方程式:________.
答案:
解析:
解析:
|
答案:(1)AgCl Cu(OH)2 BaSO4 (2)Ag++Cl- 解析:根据图示,Ba2+、Cu2+、Ag+逐一沉淀,结合所提供试剂NaOH溶液、盐酸和Na2SO4溶液,沉淀必须是最完全的,并且与所加试剂是“一一对应”的,则三种离子的沉淀顺序应为Ag+、Cu2+、Ba2+. |

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
某溶液中含有Ba2+、HCO3-、Cl-、NO3-四种离子,先向溶液中加入足量NaOH,再加入足量稀盐酸,溶液中大量减少的是( )
| A、Ba2+ | B、HCO3- | C、Cl- | D、NO3- |
 某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如右(写出最佳答案)
某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如右(写出最佳答案)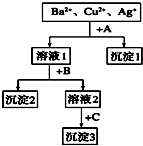 某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程如图(写出最佳答案).
某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程如图(写出最佳答案).