题目内容
从粗产品硫酸锌固体除去铁、铜、镉等可溶性硫酸盐,从而得到纯净的硫酸锌,实验流程如下: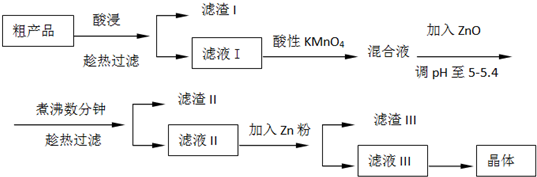
| 沉淀物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Cd(OH)2 | Mn(OH)2 | pH值 | 8.0 | 9.7 | 3.2 | 6.7 | 9.4 | 10.4 |
(1)“酸浸”步骤中,为提高锌的浸出率,可采取的措施有
(2)滤液I加入酸性KMnO4所发生反应的离子方程式为
(3)滤渣III的成份主要是
(4)从滤液III得到晶体的操作过程为
分析:(1)提高浸出率可从提高浸出速率和增加浸出时间两方面采取措施,“酸浸”要尽量降低目标产物的损失;
(2)酸性KMnO4可把亚铁离子氧化生成铁离子,调节PH值使得铁离子水解近乎完全而除掉铁离子;
(3)利用金属的置换原理除掉Mn2+、Cu2+、Cd 2+;
(4)溶液得到晶体实验操作为蒸发浓缩、冷却结晶.
(2)酸性KMnO4可把亚铁离子氧化生成铁离子,调节PH值使得铁离子水解近乎完全而除掉铁离子;
(3)利用金属的置换原理除掉Mn2+、Cu2+、Cd 2+;
(4)溶液得到晶体实验操作为蒸发浓缩、冷却结晶.
解答:解:(1)“酸浸”步骤中,为提高锌的浸出率可从提高浸出速率和增加浸出时间两方面采取措施,浸出速率越大、浸出时间越长浸出率越高,加热升高温度、增大硫酸浓度、搅拌均可提高浸出速率,“酸浸”要尽量降低目标产物的损失,因此“酸浸”时适当补充少量水的原因防止硫酸锌中从溶液中析出而损失,故答案为:增大硫酸浓度或加热升高温度或边加硫酸边搅拌或增加浸出时间;防止硫酸锌中从溶液中析出;
(2)酸性KMnO4具有强氧化性,可以把氧化亚铁离子氧化为铁离子,本身被还原为Mn2+,离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,因为Fe3++3H2O?Fe(OH)3+3H+,降低H+浓度可以使水解平衡正向移动,同时还要考虑不能引入新的杂质,所以加入ZnO,利用ZnO+2H+=Zn2++H2O不断降低H+浓度使Fe3+水解几近完全而除掉,故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;因为Fe3++3H2O?Fe(OH)3+3H+,ZnO+2H+=Zn2++H2O,加入ZnO能促进Fe3+水解生成Fe(OH)3而除去;
(3)滤液II 中含有的杂质离子有 Mn2+、Cu2+、Cd 2+,利用较活泼金属可把较不活泼金属从其盐溶液中置换出来的原理,从而达到除去三种杂质离子的目的,
故答案为:Mn、Cd、Cu;
(4)溶液得到晶体实验操作为:蒸发浓缩、冷却结晶,故答案为:蒸发浓缩.
(2)酸性KMnO4具有强氧化性,可以把氧化亚铁离子氧化为铁离子,本身被还原为Mn2+,离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,因为Fe3++3H2O?Fe(OH)3+3H+,降低H+浓度可以使水解平衡正向移动,同时还要考虑不能引入新的杂质,所以加入ZnO,利用ZnO+2H+=Zn2++H2O不断降低H+浓度使Fe3+水解几近完全而除掉,故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;因为Fe3++3H2O?Fe(OH)3+3H+,ZnO+2H+=Zn2++H2O,加入ZnO能促进Fe3+水解生成Fe(OH)3而除去;
(3)滤液II 中含有的杂质离子有 Mn2+、Cu2+、Cd 2+,利用较活泼金属可把较不活泼金属从其盐溶液中置换出来的原理,从而达到除去三种杂质离子的目的,
故答案为:Mn、Cd、Cu;
(4)溶液得到晶体实验操作为:蒸发浓缩、冷却结晶,故答案为:蒸发浓缩.
点评:本题考察学生提纯实验操作、离子除杂设计氧化还原反应、盐类水解、金属置换反应等化学反应原理,掌握上述化学反应原理是解题关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 三聚氰胺(结构简式如右)由于含氮量高而常被不法商人用作食品添加剂,因此三聚氰胺也被人称为“蛋白精”. 三聚氰胺是一种纯白色晶体,无味,常压熔点354℃(分解);快速加热升华,升华温度300℃.三聚氰胺早期合成使用双氰胺法:由电石(CaC2)在N2氛围中加热可制备氰胺化钙(CaCN2),氰胺化钙水解后二聚生成双氰胺(C2H4N4),再加热即转化为三聚氰胺.与该法相比,尿素法成本低,目前较多采用.尿素以氨气为载体,硅胶为催化剂,在380-400℃温度下沸腾反应生成三聚氰胺:6CO(NH2)2→C3N6H6+6NH3+3CO2.
三聚氰胺(结构简式如右)由于含氮量高而常被不法商人用作食品添加剂,因此三聚氰胺也被人称为“蛋白精”. 三聚氰胺是一种纯白色晶体,无味,常压熔点354℃(分解);快速加热升华,升华温度300℃.三聚氰胺早期合成使用双氰胺法:由电石(CaC2)在N2氛围中加热可制备氰胺化钙(CaCN2),氰胺化钙水解后二聚生成双氰胺(C2H4N4),再加热即转化为三聚氰胺.与该法相比,尿素法成本低,目前较多采用.尿素以氨气为载体,硅胶为催化剂,在380-400℃温度下沸腾反应生成三聚氰胺:6CO(NH2)2→C3N6H6+6NH3+3CO2. 实验化学
实验化学