题目内容
对于钠的卤化物(NaX)和硅的卤化物(SiX4),下列叙述正确的是( )
| A、SiX4难水解 |
| B、SiX4是共价化合物 |
| C、NaX易水解 |
| D、NaX的熔点一般高于SiX4 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:钠的卤化物(NaX)为离子化合物,硅的卤化物(SiX4)为共价化合物,结合离子化合物及共价化合物的性质分析.
解答:
解:A、硅的卤化物(SiX4)易水解生成硅酸和HCl,故A错误;
B、硅的卤化物(SiX4)是由非金属元素原子间通过共用电子对形成的化合物,是共价化合物,故B正确;
C、钠的强酸盐不水解,NaX(NaF除外)不易水解,故C错误;
D、钠的卤化物(NaX)为离子化合物属于离子晶体,硅的卤化物(SiX4)为共价化合物属于分子晶体,离子晶体的熔点大于分子晶体的熔点,即NaX的熔点一般高于SiX4,故D正确;
故选:BD.
B、硅的卤化物(SiX4)是由非金属元素原子间通过共用电子对形成的化合物,是共价化合物,故B正确;
C、钠的强酸盐不水解,NaX(NaF除外)不易水解,故C错误;
D、钠的卤化物(NaX)为离子化合物属于离子晶体,硅的卤化物(SiX4)为共价化合物属于分子晶体,离子晶体的熔点大于分子晶体的熔点,即NaX的熔点一般高于SiX4,故D正确;
故选:BD.
点评:本题考查了离子晶体和分子晶体的物理性质、硅的卤化物和钠的卤化物的化学性质,题目难度不大,注意根据晶体的类型来判断物质的熔点的高低.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列分离或提纯方法正确的是( )
| A、采用结晶的方法除去氯化钠溶液中的泥沙 |
| B、用酒精萃取溴水中的溴单质 |
| C、用蒸馏的方法分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃) |
| D、用过滤的方法从含有少量氯化钠溶液的硝酸钾溶液中提取硝酸钾 |
短周期中的A、B、C、D、E五种元素,原子序数依次增大.A和D,C和E分别同主族,A为非金属元素,且A与B的原子序数之和等于C的原子序数,C2-与D+的核外电子数相等.则下列说法正确的是( )
| A、B与A只能组成BA3化合物 |
| B、C、D、E形成的化合物水溶液可能显碱性 |
| C、A、B、C形成的化合物一定不能发生水解反应 |
| D、E的氧化物对应的水化物只具有氧化性 |
下列有关有机物的说法中正确的是( )
| A、所有的有机物都很容易燃烧 |
| B、乙烷不能使高锰酸钾溶液褪色 |
| C、符合同一通式的有机物一定互为同系物 |
| D、易溶于汽油、酒精、苯等有机溶剂中的物质一定是有机物 |
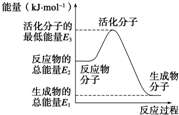 已知:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1下列说法正确的是( )
已知:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1下列说法正确的是( )| A、反应中的能量变化如图所示,则△H=E1-E3 |
| B、若加入催化剂,将改变反应历程,从而改变△H |
| C、温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1 |
| D、若保持温度和容器体积不变,充入氦气,则压强增大,化学反应速率加快 |
下列离子方程式中书写正确的是( )
| A、金属钠与水反应:Na+2H2O═Na++2OH-+H2↑ |
| B、用氢氧化钡溶液中和硫酸溶液:Ba2++SO42-═BaSO4↓ |
| C、过氧化钠与水反应:2Na2O2+2H2O═4Na++4OH-+O2↑ |
| D、向碳酸氢钠溶液中加入氢氧化钠溶液:HCO3-+OH-═H2O+CO2↑ |
丙烯醇在一定条件下可转化为丙烯醛:CH2=CHCH2OH
CH2=CHCHO.下列有关说法错误的是( )
| 新制MnO2 |
| 25℃ |
| A、丙烯醇与丙醛(CH3CH2CHO)互为同分异构体 |
| B、丙烯醇含有两种官能团 |
| C、可用新制Cu(OH)2鉴别丙烯醛和丙烯醇 |
| D、此转化过程中丙烯醇被还原 |
下列能达到实验目的是( )
A、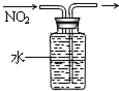 排水法收集NO2 |
B、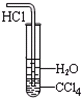 防倒吸 |
C、 实验室制氨气 |
D、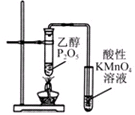 证明乙醇发生了消去反应 |