题目内容
已知下列反应:Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O (I) 5Cl2+I2+6H2O═10HCl+2HIO3 (II)
下列说法正确的是( )
下列说法正确的是( )
| A、反应I中HCl是氧化剂 |
| B、反应II 中Cl2发生氧化反应 |
| C、还原性:CoCl2>HCl>I2 |
| D、氧化性:Co2O3>Cl2>HIO3 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O中Co元素的化合价降低,Cl元素的化合价升高,
5Cl2+I2+6H2O═10HCl+2HIO3中Cl元素的化合价降低,I元素的化合价升高,结合氧化还原反应基本概念来解答.
5Cl2+I2+6H2O═10HCl+2HIO3中Cl元素的化合价降低,I元素的化合价升高,结合氧化还原反应基本概念来解答.
解答:
解:A.反应I中Cl元素的化合价升高,则HCl为还原剂,故A错误;
B.II中Cl元素的化合价降低,则氯气发生还原反应,故B错误;
C.由还原剂的还原性大于还原产物的还原性可知,I中还原性为HCl>CoCl2,II中还原性为I2>HCl,故C错误;
D.由氧化剂的氧化性大于氧化产物的氧化性可知,I中氧化性为Co2O3>Cl2,II中氧化性为Cl2>HIO3,则氧化性为Co2O3>Cl2>HIO3,故D正确;
故选D.
B.II中Cl元素的化合价降低,则氯气发生还原反应,故B错误;
C.由还原剂的还原性大于还原产物的还原性可知,I中还原性为HCl>CoCl2,II中还原性为I2>HCl,故C错误;
D.由氧化剂的氧化性大于氧化产物的氧化性可知,I中氧化性为Co2O3>Cl2,II中氧化性为Cl2>HIO3,则氧化性为Co2O3>Cl2>HIO3,故D正确;
故选D.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意氧化性、还原性比较的规律性方法,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
卤代烃能发生下列反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr下列有机物可以合成环丙烷的是( )
| A、CH3CH2CH2Br |
| B、CH3CHBrCH2Br |
| C、CH2BrCH2CH2Br |
| D、CH3CHBrCH2CH2Br |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、100mL 0.1mol?L-1的稀硫酸中含有H+个数为0.2NA |
| B、每1mol Fe被氧化,失去电子数目一定是2NA |
| C、金属钠和氧气反应制取过氧化钠,每生成1mol过氧化钠,转移电子数为4NA |
| D、Zn和稀硫酸反应,每生成1mol氢气转移电子数为2NA |
某温度和压强下,将4g由三种炔烃组成的混合气体与足量的氢气反应,充分加成后,生成4.4g三种对应的烷烃,则所得烷烃中一定有( )
| A、异丁烷 | B、乙烷 | C、丙烷 | D、丁烷 |
下列能正确表示氢气与氯气反应生成氯化氢过程中能量变化的示意图是( )
A、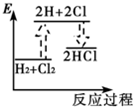 |
B、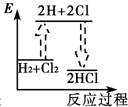 |
C、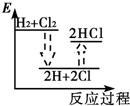 |
D、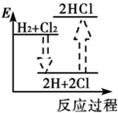 |
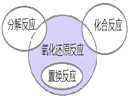 氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分
氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分的是( )
| A、4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||||
B、4NH3+5O2
| ||||
| C、2NaHCO3=Na2CO3+H2O+CO2↑ | ||||
| D、Cl2+2NaBr=2NaCl+Br2 |
下列卤代烃,既能发生水解反应,又能发生消去反应的是( )
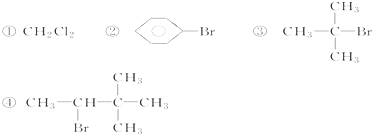

| A、①② | B、③④ | C、②④ | D、①③ |

 实验室配制欲配制480mL4.0mol?L-1的NaOH溶液.根据配置溶液的具体过程回答下列问题:
实验室配制欲配制480mL4.0mol?L-1的NaOH溶液.根据配置溶液的具体过程回答下列问题: