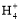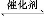ΧβΡΩΡΎ»ί
“―÷Σ¥ΉΥαΚΆ―ΈΥα «»’≥Θ…ζΜν÷–ΦΪΈΣ≥ΘΦϊΒΡΥα,‘Ύ“ΜΕ®ΧθΦΰœ¬,CH3COOH»ή“Κ÷–¥φ‘ΎΒγάκΤΫΚβ:CH3COOH CH3COO-+H+ΓΓΠΛH>0ΓΘ
CH3COO-+H+ΓΓΠΛH>0ΓΘ
(1)≥ΘΈ¬œ¬,‘ΎpH=5ΒΡœΓ¥ΉΥα»ή“Κ÷–,c(CH3COO-)=ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ(Ν– Ϋ,≤Μ±ΊΜ·Φρ);œ¬Ν–ΖΫΖ®÷–,Ω…“‘ Ι0.10 molΓΛL-1 CH3COOHΒΡΒγάκ≥ΧΕ»‘ω¥σΒΡ «ΓΓΓΓΓΓΓΓ ΓΘ
a.Φ”»κ…ΌΝΩ0.10 molΓΛL-1ΒΡœΓ―ΈΥα
b.Φ”»»CH3COOH»ή“Κ
c.Φ”Υ°œΓ Ά÷Ν0.010 molΓΛL-1
d.Φ”»κ…ΌΝΩ±υ¥ΉΥα
e.Φ”»κ…ΌΝΩ¬»Μ·ΡΤΙΧΧε
f.Φ”»κ…ΌΝΩ0.10 molΓΛL-1ΒΡNaOH»ή“Κ
(2)ΫΪΒ»÷ ΝΩΒΡ–ΩΆΕ»κΒ»ΧεΜΐ«“pHΨυΒ»”Ύ3ΒΡ¥ΉΥαΚΆ―ΈΥα»ή“Κ÷–,Ψ≠Ιΐ≥δΖ÷Ζ¥”ΠΚσ,ΖΔœ÷÷Μ‘Ύ“Μ÷÷»ή“Κ÷–”––ΩΖέ Θ”ύ,‘ρ…ζ≥…«βΤχΒΡΧεΜΐ:V(―ΈΥα)ΓΓΓΓΓΓΓΓV(¥ΉΥα),Ζ¥”ΠΒΡΉν≥θΥΌ¬ ΈΣ:v(―ΈΥα)ΓΓΓΓΓΓΓΓv(¥ΉΥα)(ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑ=Γ±)ΓΘ
(3)≥ΘΈ¬œ¬,œρΧεΜΐΈΣVa mL,pHΈΣ3ΒΡ¥ΉΥα»ή“Κ÷–ΒΈΦ”pH=11ΒΡNaOH»ή“ΚVb mL÷Ν»ή“Κ«ΓΚΟ≥ ÷––‘,‘ρVa”κVbΒΡΙΊœΒ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
(4)≥ΘΈ¬œ¬,ΫΪ0.1 mol/L―ΈΥαΚΆ0.1 mol/L¥ΉΥαΡΤ»ή“ΚΜλΚœ,ΥυΒΟ»ή“ΚΈΣ÷––‘,‘ρΜλΚœ»ή“Κ÷–ΗςάκΉ”ΒΡ≈®Ε»Α¥”…¥σΒΫ–Γ≈≈–ρΈΣΓΓ ΓΘ
(5)“―÷Σ:90 Γφ ±,Υ°ΒΡάκΉ”Μΐ≥Θ ΐΈΣKW=3.8ΓΝ10-13,‘Ύ¥ΥΈ¬Ε»œ¬,ΫΪpH=3ΒΡ―ΈΥαΚΆpH=11ΒΡ«β―θΜ·ΡΤ»ή“ΚΒ»ΧεΜΐΜλΚœ,‘ρΜλΚœ»ή“Κ÷–ΒΡc(H+)=ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ(±ΘΝτ»ΐΈΜ”––ß ΐΉ÷) mol/LΓΘ
(1)(10-5-10-9) mol/LΓΓbcf
(2)<ΓΓ=ΓΓ(3)Va<Vb
(4)c(Na+)>c(CH3COO-)>c(Cl-)>c(H+)=c(OH-)
(5)2.05ΓΝ10-11
ΓΨΫβΈωΓΩ(1)‘ΎpH=5ΒΡœΓ¥ΉΥα»ή“Κ÷–,c(H+)=10-5 mol/L,ΗυΨίΥ°ΒΡΒγάκΤΫΚβΦΑ¥ΉΥαΒΡΒγάκΤΫΚβΖΫ≥Χ ΫCH3COOH H++CH3COO-Ω…“‘Ω¥≥ω,c(CH3COO-)=c(H+)»ή“Κ-c(H+)Υ°=(10-5-10-9) mol/L;Φ”»»ΓΔΦ”Υ°œΓ ΆΓΔΦ”»κΦν–‘Έο÷ ΨυΡή ΙΒγάκΤΫΚβœρ”““ΤΕ·,Ι ―ΓbcfΓΘ
H++CH3COO-Ω…“‘Ω¥≥ω,c(CH3COO-)=c(H+)»ή“Κ-c(H+)Υ°=(10-5-10-9) mol/L;Φ”»»ΓΔΦ”Υ°œΓ ΆΓΔΦ”»κΦν–‘Έο÷ ΨυΡή ΙΒγάκΤΫΚβœρ”““ΤΕ·,Ι ―ΓbcfΓΘ
(2)¥ΉΥα «»θΥα,Β»ΧεΜΐΒ»pH,‘ρn(CH3COOH)>n(HCl),‘ρ―ΈΥα÷––ΩΖέ Θ”ύ,ΥφΉ≈ΥϋΚΆΫπ τΒΡΖ¥”Π,ΒγάκΤΫΚβ≤ΜΕœΒΊœρ”““ΤΕ·,ΜαΒγάκ≥ωΗϋΕύΒΡ«βάκΉ”,Υυ“‘¥ΉΥα≤ζ…ζΒΡ«βΤχΧεΜΐΫœ¥σ,ΩΣ Φ ±,¥ΉΥαΚΆ―ΈΥαΒΡpHΨυΒ»”Ύ3,Φ¥ΩΣ Φ ±«βάκΉ”ΒΡ≈®Ε»œύΒ»,Υυ“‘ΩΣ Φ ±ΒΡΥΌ¬ œύΒ»ΓΘ
(3)¥ΉΥα «»θΥα,pHΈΣ3ΒΡ¥ΉΥα»ή“Κ÷–,CH3COOHΒΡ≈®Ε»¥σ”Ύ10-3 mol/L,pH=11ΒΡNaOH»ή“Κ≈®Ε»Β»”Ύ10-3 mol/L,ΉνΚσ»ή“Κ«ΓΚΟ≥ ÷––‘,ΥΒΟςΦνΙΐΝΩ,Υυ“‘Va<VbΓΘ
(4)ΗυΨίΒγΚ… ΊΚψ:c(CH3COO-)+c(Cl-)+c(OH-)=c(Na+)+c(H+),»ή“ΚΈΣ÷––‘,Ω…“‘÷ΣΒάc(CH3COO-)+c(Cl-)=c(Na+),Υυ“‘c(Na+)>c(CH3COO-)>c(Cl-)>c(H+)=c(OH-)ΓΘ
(5)pH=3ΒΡ―ΈΥα÷–c(H+)=10-3 mol/L,pH=11ΒΡ«β―θΜ·ΡΤ»ή“Κ÷–:c(OH-)= =38ΓΝ10-3 mol/L,ΜλΚœΚσΦν Θ”ύ, Θ”ύΒΡ«β―θΗυΒΡ≈®Ε»ΈΣ:c(OH-)=
=38ΓΝ10-3 mol/L,ΜλΚœΚσΦν Θ”ύ, Θ”ύΒΡ«β―θΗυΒΡ≈®Ε»ΈΣ:c(OH-)= =0.018 5 mol/L,
=0.018 5 mol/L,
Υυ“‘c(H+)= mol/LΓ÷2.05ΓΝ10-11 mol/LΓΘ
mol/LΓ÷2.05ΓΝ10-11 mol/LΓΘ

 ΤΏ≤ ΧβΩ®ΩΎΥψ”Π”Ο“ΜΒψΆ®œΒΝ–¥πΑΗ
ΤΏ≤ ΧβΩ®ΩΎΥψ”Π”Ο“ΜΒψΆ®œΒΝ–¥πΑΗΑ± «ΒΣ―≠ΜΖΙΐ≥Χ÷–ΒΡ÷Ί“ΣΈο÷ ,Α±ΒΡΚœ≥… «ΡΩ«ΑΤ’±ι Ι”ΟΒΡ»ΥΙΛΙΧΒΣΖΫΖ®ΓΘ
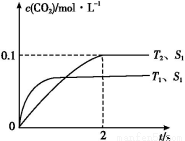
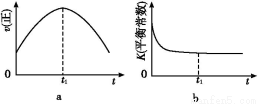
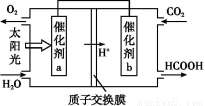
(1)ΗυΨίΆΦ1ΧαΙ©ΒΡ–≈œΔ,–¥≥ωΗΟΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ Ϋ:ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ,‘ΎΆΦ1÷–«ζœΏΓΓΓΓΓΓΓΓΓΓΓΓΓΓ(ΧνΓΑaΓ±ΜρΓΑbΓ±)±μ ΨΦ”»κΧζ¥ΞΟΫΒΡΡήΝΩ±δΜ·«ζœΏΓΘ
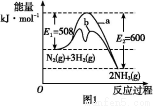
(2)‘ΎΚψ»ί»ίΤς÷–,œ¬Ν–Οη ω÷–ΡήΥΒΟς…œ ωΖ¥”Π“―¥οΤΫΚβΒΡ «ΓΓΓΓΓΓΓΓΓΘ
A.3v(H2)’ΐ=2v(NH3)Ρφ
B.ΒΞΈΜ ±ΦδΡΎ…ζ≥…n mol N2ΒΡΆ§ ±…ζ≥…2n mol NH3
C.ΜλΚœΤχΧεΒΡΟήΕ»≤Μ‘ΌΗΡ±δ
D.»ίΤςΡΎ―Ι«Ω≤ΜΥφ ±ΦδΒΡ±δΜ·Εχ±δΜ·
(3)“ΜΕ®Έ¬Ε»œ¬,œρ2 LΟή±’»ίΤς÷–≥δ»κ1 mol N2ΚΆ3 mol H2,±Θ≥÷ΧεΜΐ≤Μ±δ,0.5 minΚσ¥οΒΫΤΫΚβ,≤βΒΟ»ίΤς÷–”–0.4 mol NH3,‘ρΤΫΨυΖ¥”ΠΥΌ¬ v(N2)=ΓΓΓΓΓΓΓΓΓΓΓΓ,ΗΟΈ¬Ε»œ¬ΒΡΤΫΚβ≥Θ ΐK=ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ»τ…ΐΗΏΈ¬Ε»,K÷Β±δΜ·ΓΓΓΓΓΓΓΓ(ΧνΓΑ‘ω¥σΓ±ΓΔΓΑΦθ–ΓΓ±ΜρΓΑ≤Μ±δΓ±)ΓΘ
(4)ΈΣΝΥ―Α’“Κœ≥…NH3ΒΡΈ¬Ε»ΚΆ―Ι«ΩΒΡ “ΥΧθΦΰ,Ρ≥Ά§―ß…ηΦΤΝΥ»ΐΉι Β―ι,≤ΩΖ÷ Β―ιΧθΦΰ“―Ψ≠Χν‘Ύœ¬Οφ Β―ι…ηΦΤ±μ÷–ΓΘ
Β―ι±ύΚ≈ | T(Γφ) | n(N2)/n(H2) | p(MPa) |
ΔΓ | 450 | 1/3 | 1 |
ΔΔ | ΓΓ | ΓΓ | 10 |
ΔΘ | 480 | ΓΓ | 10 |
A.«κ‘Ύ…œ±μΩ’Ηώ÷–Χν»κ Θ”ύΒΡ Β―ιΧθΦΰ ΐΨίΓΘ
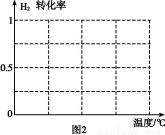
B.ΗυΨίΖ¥”ΠN2(g)+3H2(g) 2NH3(g)ΒΡΧΊΒψ,‘ΎΗχ≥ωΒΡΉχ±ξΆΦ2÷–,Μ≠≥ωΤδ‘Ύ1 MPaΚΆ10 MPaΧθΦΰœ¬H2ΒΡΉΣΜ·¬ ΥφΈ¬Ε»±δΜ·ΒΡ«ς Τ«ζœΏ Ψ“βΆΦ,≤Δ±ξΟςΗςΧθ«ζœΏΒΡ―Ι«ΩΓΘ
2NH3(g)ΒΡΧΊΒψ,‘ΎΗχ≥ωΒΡΉχ±ξΆΦ2÷–,Μ≠≥ωΤδ‘Ύ1 MPaΚΆ10 MPaΧθΦΰœ¬H2ΒΡΉΣΜ·¬ ΥφΈ¬Ε»±δΜ·ΒΡ«ς Τ«ζœΏ Ψ“βΆΦ,≤Δ±ξΟςΗςΧθ«ζœΏΒΡ―Ι«ΩΓΘ
ΒγΕΤΈέΡύ÷–Κ§”–Cr(OH)3ΓΔAl2O3ΓΔZnOΓΔCuOΓΔNiOΒ»Έο÷ ,ΙΛ“Β…œΆ®ΙΐΓΑ÷–Έ¬±Κ…’ΓΣΡΤ―θΜ·Ζ®Γ±ΜΊ ’Na2Cr2O7Β»Έο÷ ΓΘ

“―÷Σ:‘ΎNa2CrO4»ή“Κ÷–Κ§”–…ΌΝΩNaAlO2ΓΔNa2ZnO2Β»Έο÷
(1)Υ°ΫΰΚσΒΡ»ή“Κ≥ ΓΓΓΓΓΓΓΓ–‘(ΧνΓΑΥαΓ±ΓΔΓΑΦνΓ±ΜρΓΑ÷–Γ±)ΓΘ
(2)Άξ≥…―θΜ·±Κ…’Ιΐ≥Χ÷–…ζ≥…Na2CrO4ΒΡΜ·―ßΖΫ≥Χ ΫΓΘ
ΓΓΓΓΓΓΓΓCr(OH)3+ΓΓΓΓΓΓΓΓNa2CO3+ΓΓΓΓΓΓΓΓΓΓΓΓ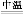 ΓΓΓΓΓΓΓΓNa2CrO4+ΓΓΓΓΓΓΓΓCO2+ΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓΓΓΓΓNa2CrO4+ΓΓΓΓΓΓΓΓCO2+ΓΓΓΓΓΓΓΓΓΓΓΓ
(3)¬Υ‘ϋΔρΒΡ÷ς“Σ≥…Ζ÷”–Zn(OH)2ΓΔΓΓΓΓΓΓΓΓΓΘ
(4)ΓΑœΒΝ–≤ΌΉςΓ±÷–ΈΣ:ΦΧ–χΦ”»κH2SO4,ΓΓΓΓΓΓΓΓ,ά以ΫαΨß,Ιΐ¬ΥΓΘΦΧ–χΦ”»κH2SO4ΡΩΒΡ «ΓΓ ΓΘ
“―÷Σ:ΔΌ≥ΐ»Ξ¬Υ‘ϋIIΚσ,»ή“Κ÷–¥φ‘Ύ»γœ¬Ζ¥”Π:
2CrO42ΓΣ+2H+ Cr2O72ΓΣ+H2O
Cr2O72ΓΣ+H2O
ΔΎNa2Cr2O7ΓΔNa2CrO4‘Ύ≤ΜΆ§Έ¬Ε»œ¬ΒΡ»ήΫβΕ»»γœ¬±μ
Έ¬Ε» »ήΫβΕ» Μ·―ß Ϋ | 20 Γφ | 60 Γφ | 100 Γφ |
Na2SO4 | 19.5 | 45.3 | 42.5 |
Na2Cr2O7 | 183 | 269 | 415 |
Na2CrO4 | 84 | 115 | 126 |
(5)ΙΛ“Β…œΜΙΩ…“‘‘ΎΥ°ΫΰΙΐ¬ΥΚσΒΡ»ή“Κ(Na2CrO4)Φ”»κ ΝΩH2SO4,”Ο ·ΡΪΉςΒγΦΪΒγΫβ…ζ≤ζΫπ τΗθ,–¥≥ω…ζ≥…ΗθΒΡΒγΦΪΖ¥”ΠΖΫ≥Χ ΫΓΓ ΓΘ