��Ŀ����
��4�֣���һ���Ϊ10L�ܱյ������У�ͨ��һ������CO��H2O��g������850��ʱ�������·�Ӧ��CO(g)+H2O(g)  CO2(g)+H2(g) ��H��0
CO2(g)+H2(g) ��H��0
��1�� CO��H2OŨ�ȱ仯��ͼ����0��4 min��ƽ����Ӧ���ʦ�(CO)��_______ mol/��L��min������ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ ��
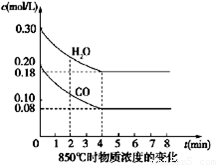
��2����������Щ���������ٷ����仯ʱ������������Ӧ�Ѵﵽƽ��״̬���� ��
A����������ѹǿ
B�����������ܶ�
C��CO�����ʵ���Ũ��
D���ܱ������зų�����
E����(CO)���(CO2)�ı�ֵ
��6�֣��������ƣ�NaClO2����һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ�����ڼ��Ի������ȶ����ڡ�ijͬѧ�������Ϻ��������NaClO2����Ҫ�������¡�
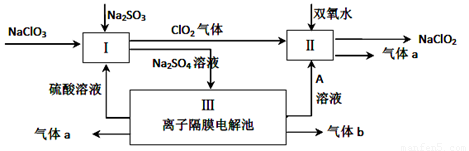
��3����ƽ���з�Ӧ����ʽ ClO3-+ H++ SO32-== ClO2��+ SO42-+
��4��A�Ļ�ѧʽ�� ������������a�ĵ缫��Ӧʽ ��
��4�֣���1��0.03����1�֣�1��1�֣���2��CD ��2�֣�
��6�֣���3��2 ClO3-+ 2 H++ 1 SO32-== 2 ClO2��+ 1SO42-+ 1 H2O ��2�֣�
��4��NaOH����2�֣���4OH-��4e-=2H2O+O2����2�֣�
��������
�����������1����=∆c��∆t=��0.20mol/l−0.08mol•L‾1����4min =0.03mol/��L•min����
������ʽ�����㣺
CO��g��ʮH2O��g�� 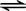 CO2��g��ʮH2 ��g��
CO2��g��ʮH2 ��g��
��ʼ��0.20mol/L 0.30mol/L 0 0
ת����0.12mol/L 0.12mol/L 0.12mol/L 0.12mol/L
ƽ�⣺0.08mol/L 0.18mol/L 0.12mol/L 0.12mol/L
��
K=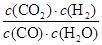 =
=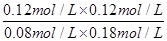 =1��
=1��
��2��A�������Ƿ�ﵽƽ�⣬���������ʵ��������䣬��������ѹǿ���䣬���ܱ����ﵽƽ�⣻B�������Ƿ�ﵽƽ�⣬�������������䣬������䣬���Ի��������ܶȲ��䲻�ܱ����ﵽƽ�⣻C����Ӧ���Ũ�Ȳ��䣬˵����Ӧ�Ѵﵽƽ�⣻D���ܱ������зų��������䣬˵����Ӧ�Ѵﵽƽ�⣻E����(CO)���(CO2)�ı�ֵ��������Ӧ���ʣ������Ƿ�ƽ�ⶼ���䣬���Բ��ܱ�����Ӧ��ƽ�⣬��CD��ȷ��
��3�����ݻ��ϼ���������ClO3‾��ClԪ����+5�۽���ΪClO2�е�+4��Cl��SO32‾��SԪ����+4�����ߵ�SO42‾��+6��S��ͨ�����ϼ������뽵����ֵ��ȿ���ƽ��ѧ����ʽ��
��4����������ͼ��֪����aΪ����������bΪ������ͬʱ����A��NaOH��OH‾ʧ��������O2���缫����ʽΪ��4OH-��4e-=2H2O+O2����
���㣺���⿼�鷴Ӧ���ʺ�ƽ�ⳣ���ļ��㡢��ѧƽ��״̬���жϡ���ѧ����ʽ����ƽ�����ԭ����

 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д�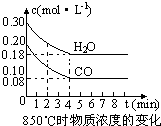 ��1����ѧƽ�ⳣ��K��ʾ���淴Ӧ�Ľ��г̶ȣ�KֵԽ��ʾ
��1����ѧƽ�ⳣ��K��ʾ���淴Ӧ�Ľ��г̶ȣ�KֵԽ��ʾ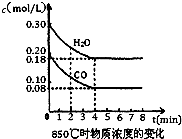 ��֪��Ӧ��CO��g��+H2O��g��?H2��g��+CO2��g����H=-41.2kJ/mol�����ɵ�CO2��H2�Բ�ͬ������Ȼ��ʱ�ں��������µķ�Ӧ���Ƶ�CH4��
��֪��Ӧ��CO��g��+H2O��g��?H2��g��+CO2��g����H=-41.2kJ/mol�����ɵ�CO2��H2�Բ�ͬ������Ȼ��ʱ�ں��������µķ�Ӧ���Ƶ�CH4��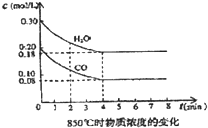 ��һ���Ϊ10L�������У�ͨ��һ������CO��H2O����85��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H=-Q kJ/mol CO��H2OŨ�ȱ仯��ͼ����
��һ���Ϊ10L�������У�ͨ��һ������CO��H2O����85��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H=-Q kJ/mol CO��H2OŨ�ȱ仯��ͼ���� ��һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ�������·�Ӧ��
��һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ�������·�Ӧ��