题目内容
在水溶液中下列电离方程式书写正确的是( )
| A.H2SO4=2H++SO42- | B.NaHCO3=Na++H++CO32- |
| C.KClO3=K++Cl-+3O2- | D.CuCl2=Cu2++Cl2- |
A、硫酸是强电解质,是强酸完全电离,H2SO4=2H++SO42-,故A正确;
B、碳酸氢根离子是弱酸阴离子,不能拆成离子,正确的是:NaHCO3=Na++HCO3-,故B错误;
C、氯酸根是算根离子,原子间通过共价键形成,不能拆成离子,正确的是:KClO3=K++ClO3-,故C错误;
D、氯化铜是2个氯离子和一个铜离子构成,正确的是:CuCl2=Cu2++2Cl-,故D错误;
故选A.
B、碳酸氢根离子是弱酸阴离子,不能拆成离子,正确的是:NaHCO3=Na++HCO3-,故B错误;
C、氯酸根是算根离子,原子间通过共价键形成,不能拆成离子,正确的是:KClO3=K++ClO3-,故C错误;
D、氯化铜是2个氯离子和一个铜离子构成,正确的是:CuCl2=Cu2++2Cl-,故D错误;
故选A.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
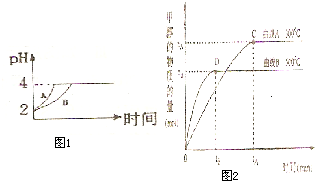 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:




