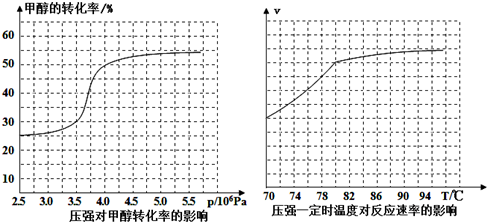
题目内容
9.某校环保小组处理污水样品,需用经过准确称量的NaOH固体配制250mL 0.2mol/L的NaOH溶液:(1)需称量的NaOH的质量是2.0g.
(2)①本实验用到的基本仪器有烧杯、天平、药匙、玻璃棒,还缺少的仪器是250mL容量瓶
胶头滴管.②定容时,如果加水超过刻度线,应该如何操作重新配制.③定容时后,倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度.对所配溶液浓度的影偏低(填“偏低”、“偏高”或“无影响”).
(3)在容量瓶的使用方法中,下列操作不正确的是B
A.使用容量瓶前检验是否漏水
B.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近标线1~2cm处,用滴管加蒸馏水至标线.
C.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀.
分析 (1)依据m=CVM计算溶质的质量;
(2)①根据配制一定物质的量浓度溶液的实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
②实验失败不能挽救的必须重新配制;
③定容时后,倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,导致溶液的体积偏大;
(3)A.为防止漏水,使用容量瓶前要检查它是否漏水;
B.容量瓶为精密仪器,不能用来溶解固体;
C.为使溶液混合均匀,定容后需要把容量瓶倒转反复上下摇匀,依据摇匀的正确操作解答.
解答 解:(1)配制250mL 0.2mol/L的NaOH溶液,需要氢氧化钠固体质量=0.2mol/L×0.25 L×40g/mol=2.0g;
故答案为:2.0g;
(2)①配制一定物质的量浓度溶液的实验操作的步骤:计算、称量、溶解、移液、洗涤、定容、摇匀等操作,用到的仪器有:托盘天平、药匙、烧杯、玻璃棒、520ml容量瓶、胶头滴管,所以还缺少的仪器是:
250mL容量瓶、胶头滴管;
故答案为:250mL容量瓶;胶头滴管;
②定容时,如果加水超过刻度线,导致实验失败且不能挽救,必须重新配制;
故答案为:重新配制;
③定容时后,倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,导致溶液的体积偏大,依据C=$\frac{n}{V}$可知,溶液浓度偏低;
故答案为:偏低;
(3)A.使用容量瓶前要检查它是否漏水,防止在配制溶液过程中漏液,故A正确;
B.配制溶液时,要先溶解稀释,冷却至室温以后,再转移至容量瓶,不能用容量瓶溶解固体,故B错误;
C.摇匀时食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转反复上下摇匀,故C正确;
故选:B.
点评 本题考查了用容量瓶配制一定物质的量浓度溶液的实验操作和注意事项,熟悉配制原理及容量瓶的构造和使用注意事项是解题关键,题目难度不大.

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案| A. | CH3CH2CH2OH+HBr$→_{H+}^{△}$CH3CH2CH2Br+H2O | |
| B. |  +NaHCO3→ +NaHCO3→ +H2CO3 +H2CO3 | |
| C. |  +CO2+H2O→ +CO2+H2O→ +NaHCO3 +NaHCO3 | |
| D. |  +3Br2→ +3Br2→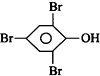 ↓+3HBr ↓+3HBr |
| A. | 蔗糖、麦芽糖互为同分异构体 | |
| B. | 常用蛋白质的颜色反应来鉴别部分蛋白质 | |
| C. | 用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 | |
| D. | 油脂在酸性或碱性条件下均能发生水解反应,且产物不同 |
| A. | 冰水混合物 | B. | 水泥 | C. | 纯净的盐酸 | D. | 普通玻璃 |
| A. | 室温下,14.0g乙烯和丁烯的混合气体中含有的C-H键数目为2NA | |
| B. | 2molSO2和1molO2在一定条件下充分反应后,所得混合气体的分子数大于2NA | |
| C. | 2.3g金属钠与过量的氧气反应,无论是否加热,转移的电子数均为0.1NA | |
| D. | 1mol Na2CO3晶体中含有的CO32-离子数小于NA |
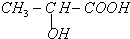 ,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
 .
.
 .
. $→_{Pd/C}^{H_{2}}$
$→_{Pd/C}^{H_{2}}$ .化合物
.化合物  是合成抗癌药物美发伦的中间体,请写出以
是合成抗癌药物美发伦的中间体,请写出以  和
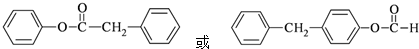
和 为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂任用).合成路线流程图示例如下: