题目内容
在密闭容器中的一定量的混合气体发生如下反应:aA(g)+bB(g)  cC(g)+dD (g)
cC(g)+dD (g)
平衡时测得A的浓度为0.5mol/L,保持温度不变,将体积压缩为原来的1/2,在达到平衡时,测得A的浓度为0.8mol/L,则下列说法正确的是: ( )
A .a+b<c+d B.平衡正向移动 C.B的转化率降低 D .C的体积分数降低
B
【解析】
试题分析:反应:aA(g)+bB(g)  cC(g)+dD (g)在平衡时测得A的浓度为0.5mol/L,保持温度不变,将体积压缩为原来的1/2,若平衡不发生移动,则达到平衡时,测得A的浓度为1.0mol/L,实际则是0.8 mol/L,则说明增大压强,平衡向正反应方向移动,根据平衡移动原理L中的压强,平衡向气体体积减小的方向移动,正反应方向是气体体积减小的方向,所以a+b>c+d,平衡正向移动,则反应物的转化率增大,生成物的平衡时的体积发生增大,因此正确说法是B。
cC(g)+dD (g)在平衡时测得A的浓度为0.5mol/L,保持温度不变,将体积压缩为原来的1/2,若平衡不发生移动,则达到平衡时,测得A的浓度为1.0mol/L,实际则是0.8 mol/L,则说明增大压强,平衡向正反应方向移动,根据平衡移动原理L中的压强,平衡向气体体积减小的方向移动,正反应方向是气体体积减小的方向,所以a+b>c+d,平衡正向移动,则反应物的转化率增大,生成物的平衡时的体积发生增大,因此正确说法是B。
考点:考查方程式中物质系数的关系、压强对平衡移动、物质的转化率、平衡含量的影响的知识。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目


 2NH3(g) ΔH=-92.4KJ/mol.他因此获得了1918年诺贝尔化学奖。在密闭容器中,使2molN2和6molH2混合发生下列反应:N2(g)+3H2(g)
2NH3(g) ΔH=-92.4KJ/mol.他因此获得了1918年诺贝尔化学奖。在密闭容器中,使2molN2和6molH2混合发生下列反应:N2(g)+3H2(g) 2NH3(g)(正反应为放热反应)
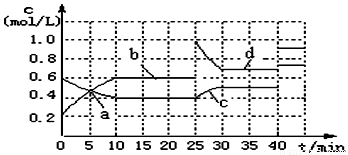
2NH3(g)(正反应为放热反应) N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )
N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )