题目内容
有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=4mol?L-1,c(HNO3)=2mol?L-1。取10mL该混合溶液与0.96g铜粉反应,标准状况下生成NO的体积为______mL。224mL
【试题分析】
解析:铜与稀硫酸、稀硝酸的混合溶液反应的实质,可用离子方程式表示为3Cu+8H++2
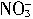 =3Cu2++2NO↑+4H2O。
=3Cu2++2NO↑+4H2O。根据n(Cu)=0.96g/64g?mol-1 =0.015mol,n(H+)=10mol?L-1×0.01L=0.1mol,n(
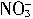 )=2mol?L-1×0.01L=0.02mol,判断可知Cu粉完全反应,H+和
)=2mol?L-1×0.01L=0.02mol,判断可知Cu粉完全反应,H+和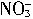 都过量。根据Cu的物质的量和离子方程式可得,n(NO)=0.015mol×2/3=0.01mol,V(NO)=224mL。
都过量。根据Cu的物质的量和离子方程式可得,n(NO)=0.015mol×2/3=0.01mol,V(NO)=224mL。 
练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案
相关题目
