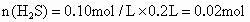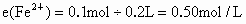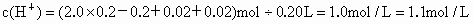题目内容
8.8g FeS固体置于200mL 2.0mol/L的盐酸中,以制备 气体
气体
![]() ,反应完全后,若溶液中
,反应完全后,若溶液中 的浓度为0.10mol/L,假定溶液体积不变.试计算:
的浓度为0.10mol/L,假定溶液体积不变.试计算:
(1)收集到的 气体的体积(标准状况).
气体的体积(标准状况).
(2)溶液中 和
和 的物质的量浓度.
的物质的量浓度.
答案:1.792L#1.792升;0.50mol/L,1.1mol/L$0.50摩尔/升,1.1摩尔/升
解析:
解析:
|
① n(FeS)=8.8g÷88g/mol=0.10moln(HCl)=0.2L ×2.0mol/L=0.4mol由 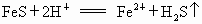 可知HCl过量,应以FeS的物质的量计算. 可知HCl过量,应以FeS的物质的量计算.
共生成 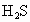 为0.10mol,在溶液中溶解的 为0.10mol,在溶液中溶解的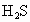 为: 为:
收集到的 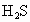 体积为: 体积为:
②生成的 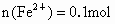
消耗的 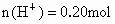 生成 生成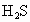 中 中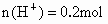
因有过量酸在,不考虑 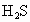 的电离 的电离 |

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目