题目内容
17.根据元素在元素周期表的位置,判断下列元素都能作为半导体材料的是( )| A. | Si K | B. | C Al | C. | As Se | D. | Si Ge |
分析 半导体材料元素既有金属性,又有非金属性,应在金属与非金属交界处.
解答 解:A、Si为半导体材料,而K是导体,故A错误;
B、C、Al都是导体,故B错误;
C、As、Se不是导体也不是半导体,故C错误;
D、Si、Ge在在金属与非金属交界处,既有金属性,又有非金属性,所以是半导体材料,故D正确;
故选D.
点评 本题考查了学生对元素周期表的熟悉程度,明确位置与性质的关系是解答的关键,题目难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
12.电石中的碳化钙和水能完全反应:CaC2+2H2O═C2H2↑+Ca(OH)2使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量.
(1)若用下列仪器和导管组装实验装置:
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是:6接3接1接5接2接4.
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞.
②检查装置的气密性.
③在仪器6和5中注入适量水.
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计).
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞.
正确的操作顺序(用操作编号填写)是②①③⑤④.
(3)若实验产生的气体有难闻的气味,且测定结果偏大,这是因为电石中含有CaS、Ca3P2杂质.
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是80%.
(1)若用下列仪器和导管组装实验装置:
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 导管及仪器 |  |  |  |  |  | 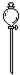 |
| 每个橡皮塞上都打了两个孔 | ||||||
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器3中,塞紧橡皮塞.
②检查装置的气密性.
③在仪器6和5中注入适量水.
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计).
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞.
正确的操作顺序(用操作编号填写)是②①③⑤④.
(3)若实验产生的气体有难闻的气味,且测定结果偏大,这是因为电石中含有CaS、Ca3P2杂质.
(4)若实验时称取的电石1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数是80%.
9.某气态烃1mol跟2mol氯化氢加成,其加成产物又可被8mol氯气完全取代,该烃可能是( )
| A. | 丙烯 | B. | 1-丁烯 | C. | 丙炔 | D. | 2-丁炔 |
7.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 6.4g 铜与S完全反应,电子转移0.1 NA个 | |
| B. | 标准状况下,2.24 L水中含有0.1 NA个水分子 | |
| C. | 1.12 L氯气中含有0.1 NA个氯原子 | |
| D. | 0.3molNO2与H2O反应转移的电子数为0.1NA |
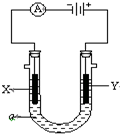 电解原理在化学工业中有广泛应用.
电解原理在化学工业中有广泛应用.
 ②Cl2
②Cl2 ③CO2
③CO2 ④H2O2
④H2O2 ⑤HClO
⑤HClO ⑥HCN
⑥HCN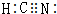
 ⑧Ca(OH)2
⑧Ca(OH)2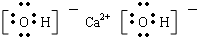 ⑨N2H4
⑨N2H4 ⑩CO(NH2)2
⑩CO(NH2)2 .
.