题目内容
磷酸盐骨水泥具有良好的生物相容性和生物活性.医药工业利用共沉淀原理,通过控制Ca与P物质的量比
制备相应产品[Ca5(PO4)3OH和Ca3(PO4)2的
分别为1.67和15]流程如图:(注:Ca5(PO4)3OH和Ca3(PO4)2和CaHPO4均难溶于水;Ca(H2 PO4)2溶液pH<7)

下表为
=1.5时,不同pH值制得滤饼的产率以及分析结果:
(1)流程中强调“滴加速度100mL/45min的作用是 .流程中调pH选氨水,不选生石灰或石灰乳的理由是 .
(2)从表中数据分析生成Ca3(PO4)2时,“pH=x”中的x的最佳取值为 ,滤饼的化学成分Ca5(PO4)3OH、Ca3(PO4)2和CaHPO4和 .
(3)酸性条件下产率偏低的原因是 .
(4)“高温煅烧”滤饼,化学反应方程式为 .
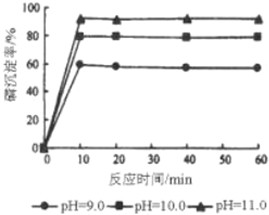
(5)下图是生产羟基磷灰石时得到的实验曲线,依据图上信息计算磷的初始浓度为0.70mmol/L,pH=10.0条件下反应前10min内磷的沉淀速率为 .
| n(Ca) |
| n(P) |
| n(Ca) |
| n(P) |

下表为
| n(Ca) |
| n(P) |
| PH值 | 6.8 | 7.2 | 8.0 | 9.0 | 10.0 | ||
| 产率(%) | 92.6 | 95.3 | 96.7 | 94.6 | 95.6 | ||
|
1.51 | 1.50 | 1.51 | 1.52 | 1.52 |
(2)从表中数据分析生成Ca3(PO4)2时,“pH=x”中的x的最佳取值为
(3)酸性条件下产率偏低的原因是
(4)“高温煅烧”滤饼,化学反应方程式为
(5)下图是生产羟基磷灰石时得到的实验曲线,依据图上信息计算磷的初始浓度为0.70mmol/L,pH=10.0条件下反应前10min内磷的沉淀速率为

考点:物质分离和提纯的方法和基本操作综合应用,难溶电解质的溶解平衡及沉淀转化的本质
专题:实验设计题
分析:(1)滴加速度较慢,可以使混合物充分接触;根据对
的影响分析;
(2)根据
的值,及产率综合分析;根据反应物判断滤饼的化学成分;
(3)酸性条件下易生成可溶性的Ca(H2PO4)2;
(4)高温下,CaHPO4与CaCO3反应生成Ca3(PO4)2;
(5)根据图可知pH=10.0条件下,磷的沉淀率为80%,根据v=
计算.
| n(Ca) |
| n(P) |
(2)根据
| n(Ca) |
| n(P) |
(3)酸性条件下易生成可溶性的Ca(H2PO4)2;
(4)高温下,CaHPO4与CaCO3反应生成Ca3(PO4)2;
(5)根据图可知pH=10.0条件下,磷的沉淀率为80%,根据v=
| △c |
| t |
解答:
解:(1)滴加速度较慢,可以使混合物充分接触,所以滴加速度100mL/45min的作用是使反应物充分接触;流程中调pH选氨水,不选生石灰或石灰乳,是因为生石灰或石灰乳能增大钙离子的浓度,会改变
;
故答案为:使反应物充分接触;若选择生石灰或石灰乳调节PH会改变
;
(2)当PH=7.2,
=1.5时,Ca与P恰好为3:2,符合Ca3(PO4)2中Ca与P的比例,此时产率较高,所以选择PH=7.2;已知反应物为(NH4)2HPO4、NH4HCO3、Ca(NO3)2,所以滤饼的化学成分为Ca5(PO4)3OH、Ca3(PO4)2、CaHPO4和CaCO3,
故答案为:7.2;CaCO3;
(3)酸性条件下易生成可溶性的Ca(H2PO4)2,造成钙、磷的流失;故答案为:酸性条件下,容易造成钙的流失;
(4)高温下,CaHPO4与CaCO3反应生成Ca3(PO4)2,其反应的方程式为:2CaHPO4+CaCO3
Ca3(PO4)2+CO2↑+H2O;
故答案为:2CaHPO4+CaCO3
Ca3(PO4)2+CO2↑+H2O;
(5)根据图可知pH=10.0条件下,磷的沉淀率为80%,磷的初始浓度为0.70mmol/L,则反应的量为0.70mmol/L×80%=0.56mmol/L,
则v=
=
=0.056mmol/(L?min);
故答案为:0.056mmol/(L?min).
| n(Ca) |
| n(P) |
故答案为:使反应物充分接触;若选择生石灰或石灰乳调节PH会改变
| n(Ca) |
| n(P) |
(2)当PH=7.2,
| n(Ca) |
| n(P) |
故答案为:7.2;CaCO3;
(3)酸性条件下易生成可溶性的Ca(H2PO4)2,造成钙、磷的流失;故答案为:酸性条件下,容易造成钙的流失;
(4)高温下,CaHPO4与CaCO3反应生成Ca3(PO4)2,其反应的方程式为:2CaHPO4+CaCO3
| ||
故答案为:2CaHPO4+CaCO3
| ||
(5)根据图可知pH=10.0条件下,磷的沉淀率为80%,磷的初始浓度为0.70mmol/L,则反应的量为0.70mmol/L×80%=0.56mmol/L,
则v=
| △c |
| t |
| 0.56mmol/L |
| 10min |
故答案为:0.056mmol/(L?min).
点评:本题考查了钙磷形成化合物的性质,涉及物质的制备、反应速率的计算、方程式的书写等,题目难度中等,注意对表格数据及图象的分析利用.

练习册系列答案
相关题目
某无色透明溶液能与铝粉反应放出H2,则此溶液中一定能大量共存的离子组为( )
| A、OH-、Na+、K+、MnO4- |
| B、H+、Cl-、Ba2+、NO3- |
| C、K+、Cl-、Na+、SO42- |
| D、NH4+、Mg2+、Cl-、HCO3- |
由-OH、-CH3、-C6H5、-COOH四种基团两两组合(包括同种基团间的组合)形成的物质中,属于有机物且水溶液显酸性的有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
下列叙述正确的是( )
| A、离子化合物中可能含有共价键 |
| B、共价化合物中可能还有离子键 |
| C、两种元素组成的分子中一定只有极性键 |
| D、非金属元素组成的化合物一定是共价化合物 |
