题目内容
 如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )
如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )
| 选项 | 发生装置中的药品 | 干燥和集气装置 |
| A | 电石和饱和食盐水 | 图2 |
| B | 大理石和稀盐酸 | 图1 |
| C | 铜和稀硝酸 | 图2 |
| D | 氧化钙和浓氨水 | 图1 |
| A、A | B、B | C、C | D、D |
考点:常见气体制备原理及装置选择
专题:实验题
分析:图1装置的特点是:气体能用碱石灰干燥,气体可用向下排空气法收集;图2装置的特点是:气体能用氯化钙干燥,气体可用向上排空气法收集.
解答:
解:A、乙炔的密度略小于空气的密度,所以不能用排气法收集,应采用排水法收集,故A错误.
B、大理石和稀盐酸反应生成二氧化碳,二氧化碳气体和碱石灰反应,所以不能用碱石灰干燥,且二氧化碳的密度大于空气的密度,应采用向上排空气法收集,故B错误.
C、铜和稀硝酸反应生成NO,一氧化氮能和氧气反应生成二氧化氮,所以不能用排空气法收集,故C错误.
D、氨气和碱石灰不反应,所以可用碱石灰干燥,氨气的密度小于空气的密度,所以可用向下排空气法收集,故D正确.
故选D.
B、大理石和稀盐酸反应生成二氧化碳,二氧化碳气体和碱石灰反应,所以不能用碱石灰干燥,且二氧化碳的密度大于空气的密度,应采用向上排空气法收集,故B错误.
C、铜和稀硝酸反应生成NO,一氧化氮能和氧气反应生成二氧化氮,所以不能用排空气法收集,故C错误.
D、氨气和碱石灰不反应,所以可用碱石灰干燥,氨气的密度小于空气的密度,所以可用向下排空气法收集,故D正确.
故选D.
点评:本题考查常见气体的干燥和收集,做题时要充分考虑物质的性质,认真分析实验装置图的特点,从而做出正确判断,题目难度不大.

练习册系列答案
相关题目
下列四种粒子的结构示意图中,属于稀有气体元素的原子是( )
A、 |
B、 |
C、 |
D、 |
在共价化合物中,元素化合价有正负的主要原因是( )
| A、电子有得失 |
| B、共用电子对有偏移 |
| C、电子既有得失又有电子对偏移 |
| D、有金属元素的存在 |
已知离子 bX3+ 的离子结构示意图为: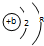 ,下列认识正确的是( )
,下列认识正确的是( )
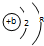 ,下列认识正确的是( )
,下列认识正确的是( )| A、b=10 |
| B、X单质能溶于氢氧化钠溶液 |
| C、X为稀有气体 |
| D、X单质既具有还原性,又具有氧化性 |
下列关于浓硫酸和稀硫酸的叙述中正确的是( )
| A、都能作干燥剂 |
| B、加热时都能与铜发生反应 |
| C、都具有一定的氧化性 |
| D、在常温下都能用铁制容器贮存 |
下列说法不正确的是( )
| A、活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同 |
| B、同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积不相等 |
| C、将SO2气体通入BaCl2溶液中至饱和,未见沉淀生成,继续通入NO2则有沉淀生成 |
| D、除FeCl2溶液中的少量FeCl3,可用加入足量铁屑过滤的方法 |
相同物质的量浓度的NaCN 和NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN和HClO说法正确的是( )
| A、酸根离子浓度:c(CNˉ)<c(ClOˉ) |
| B、电离程度:HCN>HClO |
| C、pH:HClO>HCN |
| D、与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
已知有如下反应:
①2BrO
+Cl2═Br2+2ClO
;
②ClO
+5Cl-+6H+═3Cl2+3H2O;
③2FeCl3+2KI═2FeCl2+2KCl+I2;
④2FeCl2+Cl2═2FeCl3.
下列叙述正确的是( )
①2BrO
- 3 |
- 3 |
②ClO
- 3 |
③2FeCl3+2KI═2FeCl2+2KCl+I2;
④2FeCl2+Cl2═2FeCl3.
下列叙述正确的是( )
A、氧化能力:ClO
| ||||
| B、还原能力:Fe2+>I->Cl- | ||||
C、反应ClO
| ||||
D、氧化能力:BrO
|