题目内容
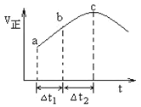
【题目】T℃时,在20.00mL0.10mol·L-1的一元酸HR溶液中滴入0.10mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的关系如图所示。

下列说法不正确的是( )
A..T℃时,HR电离常数Ka≈1.0×10-5
B.M点对应的NaOH溶液体积为20.00mL
C.N点与Q点所示溶液中水的电离程度:N>Q
D.M点所示溶液中c(Na+)=c(R-)
【答案】B
【解析】
A.P点溶液的pH=3,则c(H+)=1×10-3mol/L,c(R-)≈c(H+),c(HR)≈0.1mol/L,则T℃时HR电离平衡常数Ka=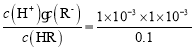 =1.0×10-5,故A正确;
=1.0×10-5,故A正确;
B.M点溶液的pH=7,则溶液呈中性,此时c(H+)= c(OH-),而HR与氢氧化钠反应完全生成的NaR溶液呈碱性,所以溶液显中性时氢氧化钠的体积应小于20ml,故B错误;
C.N点HR可能恰好完全反应,也可能氢氧化钠稍微过量,但无论何种情况,Q点溶液中氢氧化钠的浓度要大于N点,碱的电离抑制水的电离,则水的电离程度:N>Q,故C正确;
D.M点溶液中存在电荷守恒c(OH-)+c(R-)=c(H+)+(Na+),溶液显中性,则c(OH-)=c(H+),所以c(R-)=(Na+),故D正确;
故答案为B。

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目