题目内容
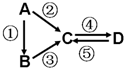 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体.写④反应离子方程式
(2)若A是太阳能电池用的光伏材料.C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性.写出②反应的化学方程式
(3)若A是应用最广泛的金属.④反应用到A,②⑤反应均用到同一种非金属单质.C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式
考点:无机物的推断
专题:推断题
分析:(1)若D物质具有两性,含有Al元素,则A为Al,④反应是通入过量的一种引起温室效应的主要气体,说明C为偏铝酸盐,D为Al(OH)3,②③反应均要用强碱溶液,B为氧化铝或铝盐,据此解答;
(2)若A是太阳能电池用的光伏材料,则A为Si,C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性,说明盐水解呈碱性,可推知C为Na2SiO3,D为Na2CO3,B为SiO2;
(3)若A是应用最广泛的金属,则A为Fe,④反应用到A,②⑤反应均用到同一种非金属单质,C的溶液用于蚀刻印刷铜电路板,含有铁离子,则非金属性单质为Cl2,可推知C为FeCl3,D为FeCl2.
(2)若A是太阳能电池用的光伏材料,则A为Si,C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性,说明盐水解呈碱性,可推知C为Na2SiO3,D为Na2CO3,B为SiO2;
(3)若A是应用最广泛的金属,则A为Fe,④反应用到A,②⑤反应均用到同一种非金属单质,C的溶液用于蚀刻印刷铜电路板,含有铁离子,则非金属性单质为Cl2,可推知C为FeCl3,D为FeCl2.
解答:
解:(1)若D物质具有两性,含有Al元素,则A为Al,④反应是通入过量的一种引起温室效应的主要气体,说明C为偏铝酸盐,D为Al(OH)3,②③反应均要用强碱溶液,B为氧化铝或铝盐,则:反应④的离子方程式为:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-,
故答案为:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-;
(2)若A是太阳能电池用的光伏材料,则A为Si,C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性,说明盐水解呈碱性,可推知C为Na2SiO3,D为Na2CO3,B为SiO2,则:②的反应的化学方程式为:Si+2NaOH+H2O=Na2SiO3+2H2↑,
故答案为:Si+2NaOH+H2O=Na2SiO3+2H2↑;Na2CO3;
(3)若A是应用最广泛的金属,则A为Fe,④反应用到A,②⑤反应均用到同一种非金属单质,C的溶液用于蚀刻印刷铜电路板,含有铁离子,则非金属性单质为Cl2,可推知C为FeCl3,D为FeCl2,C的溶液用于蚀刻印刷铜电路板反应的离子方程式为:Cu+2Fe3+=Cu2++2Fe2+,
故答案为:Cu+2Fe3+=Cu2++2Fe2+.
故答案为:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-;
(2)若A是太阳能电池用的光伏材料,则A为Si,C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性,说明盐水解呈碱性,可推知C为Na2SiO3,D为Na2CO3,B为SiO2,则:②的反应的化学方程式为:Si+2NaOH+H2O=Na2SiO3+2H2↑,
故答案为:Si+2NaOH+H2O=Na2SiO3+2H2↑;Na2CO3;
(3)若A是应用最广泛的金属,则A为Fe,④反应用到A,②⑤反应均用到同一种非金属单质,C的溶液用于蚀刻印刷铜电路板,含有铁离子,则非金属性单质为Cl2,可推知C为FeCl3,D为FeCl2,C的溶液用于蚀刻印刷铜电路板反应的离子方程式为:Cu+2Fe3+=Cu2++2Fe2+,
故答案为:Cu+2Fe3+=Cu2++2Fe2+.
点评:本题考查了无机物的推断,涉及Al、Si、Fe元素单质化合物性质,需要学生熟练掌握元素化合物知识,难度不大.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案
相关题目
关于乙酸的性质叙述正确的是( )
| A、它是四元酸 |
| B、清洗大理石的建筑物用醋酸溶液 |
| C、它的酸性较弱,能使酸碱指示剂变色 |
| D、它的晶体里有冰,所以称为冰醋酸 |
欲将NaCl中混有的少量碳铵和砂子(SiO2)除去,所进行的必要分离方法是( )
| A、溶解、过滤、萃取 |
| B、加热、溶解、过滤 |
| C、升华、萃取、分液 |
| D、盐析、渗析、纸上层析 |