题目内容
将54.4g铁粉和氧化铁的混合物中加入200mL的稀硫酸,恰好完全反应,放出氢气4.48L(标准状况).反应后的溶液中滴加KSCN不显红色,且无固体剩余物,求:
(1)混合物铁和氧化铁各是多少克?
(2)原稀硫酸物质的量浓度?
(3)反应后得到FeSO4的物质的量是多少?
(1)混合物铁和氧化铁各是多少克?
(2)原稀硫酸物质的量浓度?
(3)反应后得到FeSO4的物质的量是多少?
考点:有关混合物反应的计算
专题:计算题
分析:铁粉和氧化铁的混合物中加入稀硫酸,恰好完全反应,放出氢气,反应后的溶液中滴加KSCN不显红色,且无固体剩余物,则最终溶液中溶质为FeSO4,发生反应:Fe+Fe2O3+3H2SO4=3FeSO4+3H2O、Fe+H2SO4=FeSO4+H2↑,计算生成4.48L氢气时消耗Fe、H2SO4的物质的量,设原混合物中Fe2O3的物质的量为xmol,根据化学方程式表示出与氧化铁反应消耗Fe、H2SO4的物质的量,再根据混合物总质量列方程计算.
(1)根据m=nM计算混合物铁和氧化铁的质量;
(2)根据n=
计算硫酸的物质的量浓度;
(3)根据硫酸根离子守恒计算FeSO4的物质的量.
(1)根据m=nM计算混合物铁和氧化铁的质量;
(2)根据n=
| n |
| V |
(3)根据硫酸根离子守恒计算FeSO4的物质的量.
解答:
解:铁粉和氧化铁的混合物中加入稀硫酸,恰好完全反应,放出氢气,反应后的溶液中滴加KSCN不显红色,且无固体剩余物,则最终溶液中溶质为FeSO4,
反应生成 H2的物质的量为:
=0.2mol,则:
Fe+H2 SO4=FeSO4+H2↑
0.2mol 0.2mol 0.2mol
设原混合物中Fe2O3的物质的量为xmol,则:
Fe+Fe2O3+3H2SO4=3FeSO4+3H2O
x mol x mol 3x mol
由题意可知,(x+0.2)mol×56g/mol+x mol×160g/mol=54.4g,
解得x=0.2mol,
(1)混合物中m(Fe2O3)=0.2 mol×160 g?mol-1=32 g,m(Fe)=54.4g-32g=22.4g,
答:铁的质量为22.4g,氧化铁的质量为32g.
(2)n(H2SO4)=(3x+0.2)mol=(3×0.2+0.2)mol=0.8mol,则c(H2SO4)=
=4mol/L
答:原稀硫酸的浓度为4mol/L.
(3)根据硫酸根守恒:n(FeSO4)=n(H2SO4)=0.8mol,
答:生成硫酸亚铁的物质的量为0.8mol.
反应生成 H2的物质的量为:
| 4.48L |
| 22.4L/mol |
Fe+H2 SO4=FeSO4+H2↑
0.2mol 0.2mol 0.2mol
设原混合物中Fe2O3的物质的量为xmol,则:
Fe+Fe2O3+3H2SO4=3FeSO4+3H2O
x mol x mol 3x mol
由题意可知,(x+0.2)mol×56g/mol+x mol×160g/mol=54.4g,
解得x=0.2mol,
(1)混合物中m(Fe2O3)=0.2 mol×160 g?mol-1=32 g,m(Fe)=54.4g-32g=22.4g,
答:铁的质量为22.4g,氧化铁的质量为32g.
(2)n(H2SO4)=(3x+0.2)mol=(3×0.2+0.2)mol=0.8mol,则c(H2SO4)=
| 0.8mol |
| 0.2L |
答:原稀硫酸的浓度为4mol/L.
(3)根据硫酸根守恒:n(FeSO4)=n(H2SO4)=0.8mol,
答:生成硫酸亚铁的物质的量为0.8mol.
点评:本题考查混合物计算,明确发生的反应是解题关键,注意根据方程式解答,侧重考查学生的分析思维能力,难度中等.

练习册系列答案
相关题目
下列物质不能发生加成反应的是( )
| A、C2H4Br2 |
| B、C2H4 |
| C、C2H6 |
| D、C2H2 |
下列既可以是原电池发生的电极反应式,又可以是电解池发生的电极反应式的是( )
①Cu-2e-=Cu2+ ②4OH--4e-=2H2O+O2↑ ③2H++2e-=H2↑
④Cu2++2e-=Cu ⑤2I--2e-=I2 ⑥2H2O+O2+4e-=4OH-.
①Cu-2e-=Cu2+ ②4OH--4e-=2H2O+O2↑ ③2H++2e-=H2↑
④Cu2++2e-=Cu ⑤2I--2e-=I2 ⑥2H2O+O2+4e-=4OH-.
| A、①②④⑥ | B、②③④⑤ |
| C、①③④ | D、②④⑥ |
 霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物.下列说法正确的是( )
霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物.下列说法正确的是( )| A、MMF能溶于水 |
| B、1 mol MMF能与含3 mol NaOH的水溶液完全反应 |
| C、1 mol MMF能与6 mol氢气发生加成反应 |
| D、MMF能发生取代反应和消去反应 |

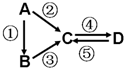 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系: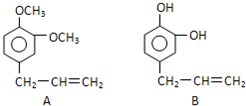 从某些植物树叶提取的挥发油中含有下列主要成分:
从某些植物树叶提取的挥发油中含有下列主要成分: