题目内容
4.下列各组元素中,已知A、B两种元素的原子序数,其中可组成AB3型离子化合物的是( )| A. | 6和9 | B. | 13和9 | C. | 11和8 | D. | 12和17 |
分析 A、B两种元素可以组成AB3型离子化合物,A属于金属元素、B属于非金属元素,则A位于第ⅢA族、B位于第VⅡA族,据此分析解答.
解答 解:A.6和9号元素分别为C、F,不能形成离子化合物,故A错误;
B.13和9分别为Al和F,可形成AB3型离子化合物,故B正确;
C.11和8号元素分别为Na和O形成氧化钠和过氧化钠,不是AB3型离子化合物,故C错误;
D.分别为Mg和Cl,形成MgCl2,故D错误.
故选B.
点评 本题考查原子结构和元素性质,熟练掌握原子结构、元素周期表结构及常见元素化合价,知道离子化合物与共价化合物的区别,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.将ag水煤气(成分为CO和H2)充分燃烧,将燃烧生成的气体(150℃)通过盛有过量的Na2O2的干燥管(反应气体无损失),充分反应后干燥管增重bg,则a和b的关系为( )
| A. | a=b | B. | a>b | C. | a<b | D. | 无法比较 |
12.下列表示对应化学反应的离子方程式或化学方程式正确的是( )
| A. | 向NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 向NaAlO2溶液中通入过量CO2:2 AlO+CO2+3H2O═2Al(OH)3↓+CO | |
| D. | 以下有机物在碱性条件下水解的化学方程式: |
19.下列说法正确的是( )
| A. | 铅笔芯的原材料为铅,儿童使用铅笔时如果用嘴吮咬能够引起铅中毒 | |
| B. | 酸雨形成的主要原因是汽车尾气的任意排放 | |
| C. | 维生素C受热更易被氧化,故有些新鲜蔬菜生吃较好 | |
| D. | 淀粉、纤维素,、蛋白质和油脂均属于天然高分子化合物 |
9.已知31g白磷变成红磷放出18.39kJ热量,下列两反应中:
P4(s)+5O2(g)═2P2O5(s)△H=Q1 kJ•mol-1
4P(红,s)+5O2(g)═2P2O5(s)△H=Q2kJ•mol-1
则下列说法中正确的是( )
P4(s)+5O2(g)═2P2O5(s)△H=Q1 kJ•mol-1
4P(红,s)+5O2(g)═2P2O5(s)△H=Q2kJ•mol-1
则下列说法中正确的是( )
| A. | Q1>Q2,白磷比红磷稳定 | B. | Q1>Q2,红磷比白磷稳定 | ||
| C. | Q1<Q2,白磷比红磷稳定 | D. | Q1<Q2,红磷比白磷稳定 |
13.下列说法中正确的是( )
| A. | 升高温度只能加快吸热反应的速率 | |
| B. | 对于任何反应,增大压强都可以加快反应速率 | |
| C. | 颗粒小的大理石和颗粒大的大理石跟同浓度的盐酸反应,前者反应速率快,是由于碳酸钙浓度大的缘故 | |
| D. | 催化剂能使可逆反应的正、逆反应速率同时加快 |
14.实验中需0.1mol•L-1的Na2CO3溶液950mL,用容量瓶配制时应称取Na2CO3粉末的质量为( )
| A. | 10.6g | B. | 10.1g | C. | 10.07g | D. | 12.0g |

 ;
; 、
、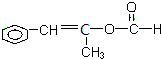 、
、 ;
; +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +NaCl+2H2O.
+NaCl+2H2O.