题目内容
化学在药物的合成和使用中起着至关重要的作用.已知:A俗名小苏打,可用于治疗胃酸过多症,中和胃酸时会产生气体;B是两性氢氧化物,也可用来制作胃药,但中和胃酸时没有气体放出.回答下列问题:
(1)B是 (填化学式)
(2)A中和胃酸的离子方程式为
(3)写出在实验室里制取B的离子方程式为 .
(1)B是
(2)A中和胃酸的离子方程式为
(3)写出在实验室里制取B的离子方程式为
考点:镁、铝的重要化合物,钠的重要化合物
专题:几种重要的金属及其化合物
分析:小苏打是碳酸氢钠的俗称,可以和盐酸反应生成氯化钠、水以及二氧化碳,氢氧化铝是两性氢氧化物,既能和强酸反应又能和强碱反应,所以制取氢氧化铝用可溶性的铝盐和氨水反应.
解答:
解:(1)小苏打是碳酸氢钠的俗称,氢氧化铝是两性氢氧化物,都可用来制作胃药,B为Al(OH)3;
故答案为:Al(OH)3;
(2)碳酸氢钠可以和盐酸反应生成氯化钠、水以及二氧化碳,即NaHCO3+HCl=NaCl+CO2↑+H2O,离子反应方程式为:HCO3-+H+=CO2↑+H2O;
故答案为:HCO3-+H+=CO2↑+H2O;
(3)氢氧化铝是两性氢氧化物,能和强碱反应,所以制取氢氧化铝时用可溶性的铝盐和氨水反应来制取,即Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+.
故答案为:Al(OH)3;
(2)碳酸氢钠可以和盐酸反应生成氯化钠、水以及二氧化碳,即NaHCO3+HCl=NaCl+CO2↑+H2O,离子反应方程式为:HCO3-+H+=CO2↑+H2O;
故答案为:HCO3-+H+=CO2↑+H2O;
(3)氢氧化铝是两性氢氧化物,能和强碱反应,所以制取氢氧化铝时用可溶性的铝盐和氨水反应来制取,即Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+.
点评:本题考查学生碳酸氢钠以及含铝化合物的性质知识,注意知识的归纳和整理是解题的关键,难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)═2NH3(g)△H=-92.6kJ/mol
实验测得起始、平衡时的有关数据如下表:
下列叙述错误的是( )
N2(g)+3H2(g)═2NH3(g)△H=-92.6kJ/mol
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A、容器①、②中反应的平衡常数相等 |
| B、平衡时,两个容器中NH3的体积分数相等 |
| C、容器②中达平衡时放出的热量Q=23.15 kJ |
| D、若容器①体积为0.5 L,则平衡时放出的热大于23.15 kJ |
 在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
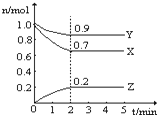 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白: