题目内容
12.下列有关物质性质的应用正确的是( )| A. | 铜的金属活动性比铁差,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| B. | 铵盐受热易分解,实验室常加热硝酸铵与氢氧化钙的混合物制取氨气 | |
| C. | 氯化铁有氧化性,工业上用FeCl3溶液蚀刻铜箔制造电路板 | |
| D. | 氨水具有弱碱性,可与饱和氯化铁溶液反应制得氢氧化铁胶体 |
分析 A、根据牺牲阳极的阴极保护法来保护金属;
B、硝酸铵受热易分解爆炸;
C、FeCl3能和铜反应;
D、FeCl3和氨水生成的是氢氧化铁沉淀.
解答 解:A、将铜连在轮船上,则铜做正极,轮船做负极,会加快轮船的腐蚀;因要减缓船体的腐蚀应连接比铁更活泼的金属,如锌,这就是牺牲阳极的阴极保护法,故A错误;
B、铵盐与碱反应生成氨气需要加热,而硝酸铵受热易分解爆炸,所以不能用硝酸铵与碱加热反应制备氨气,实验室常加热氯化铵与氢氧化钙的混合物制备氨气,故B错误;
C、FeCl3能和铜反应:2FeCl3+Cu=2FeCl2+CuCl2,故能腐蚀印刷电路板,故C正确;
D、FeCl3和氨水生成的是氢氧化铁沉淀,得到的不是胶体,要想得到胶体,应将氯化铁溶液滴入沸水中,故D错误.
故选C.
点评 本题考查了铵盐的性质、氨气的制备、钢铁的腐蚀防护,题目难度不大,属于基础性知识的考查,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
3.下列液体均处于25℃,有关叙述正确的是( )
| A. | pH=4.0的番茄汁中c(H+)是pH=6.0的牛奶中c(H+)的100倍 | |
| B. | 强电解质溶液的导电性一定比弱电解质溶液的导电性强 | |
| C. | AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 | |
| D. | pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-) |
20.甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究.
(1)B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O.
(2)A中溶液变红的原因是Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化钾,所以溶液变红.
(3)为了探究现象II的原因,甲同学进行如下实验.
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液,甲同学的实验证明产生现象II的原因是SCN-与Cl2发生了反应.
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为 .
.
①同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素.
③通过实验证明了SCN-中氮元素转化为NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成NO3-
④SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol.
| 操 作 | 现 象 |
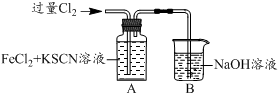 | I.A中溶液变红 II.稍后,溶液由红色变为黄色 |
(2)A中溶液变红的原因是Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的硫氰化钾,所以溶液变红.
(3)为了探究现象II的原因,甲同学进行如下实验.
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在Fe3+.
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液,甲同学的实验证明产生现象II的原因是SCN-与Cl2发生了反应.
(4)甲同学猜想SCN-可能被Cl2氧化了,他又进行了如下研究.
资料显示:SCN-的电子式为
 .
.①同学认为SCN-中碳元素没有被氧化,理由是SCN-中的碳元素是最高价态+4价.
②A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素.
③通过实验证明了SCN-中氮元素转化为NO3-,他的实验方案是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,证明A中存在,SCN-中氮元素被氧化成NO3-
④SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol.
7.稀氨水中存在电离平衡:NH3•H2O?NH4++OH-,若要使平衡正向移动,同时使c(OH-)减小,应加入的物质或采取的措施是( )①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热 ⑥加入少量MgSO4固体.
| A. | ①②⑤ | B. | ③⑥ | C. | ①②④ | D. | ②④⑤⑥ |
4.下列说法中,不正确的是( )
| A. | 肉类富含蛋白质,属于碱性食物 | |
| B. | 碳酸氢钠可用于治疗胃酸过多 | |
| C. | 碘是人体必需的微量元素之一 | |
| D. | 食用富含维生素C的水果有益于身体健康 |
1.下列反应完毕后有沉淀的是( )
| A. | KOH 溶液与FeCl3 溶液加足量稀硝酸 | |
| B. | Ba(OH)2 溶液与KNO3溶液加足量H2SO4 | |
| C. | CuSO4溶液与NaOH 溶液加足量稀盐酸 | |
| D. | BaCl2 溶液与Na2CO3 溶液加足量稀醋酸 |
 一定温度下,将0.4mol SO2和0.2mol O2放入固定容积为2L的密闭容器中,发生反应2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ/mol,反应中SO3的物质的量浓度的变化情况如图:
一定温度下,将0.4mol SO2和0.2mol O2放入固定容积为2L的密闭容器中,发生反应2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ/mol,反应中SO3的物质的量浓度的变化情况如图:

 (或
(或
 ).
).