题目内容
在一定条件下,将64 g SO2气体和32g氧气通入密闭容器中生成SO3气体,达到平衡时,共放出热量78.64KJ,已知SO2在此条件下转化率为80%,则下列热化学方程式正确的是
A.SO2(g)+1/2O2(g)![]() SO3(g);△H=-78.64KJ·mol-1
SO3(g);△H=-78.64KJ·mol-1
B.2SO2(g)+O2(g)![]() 2SO3(g);△H=-196.6KJ·mol-1
2SO3(g);△H=-196.6KJ·mol-1
C.SO2(g)+1/2O2(g)![]() SO3(l);△H=-98.3KJ·mol-1
SO3(l);△H=-98.3KJ·mol-1
D.2SO2(g)+O2(g)![]() 2SO3(g); △H=+196.6KJ·mol-1
2SO3(g); △H=+196.6KJ·mol-1
B

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
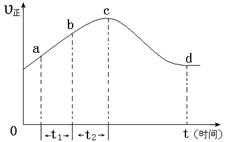
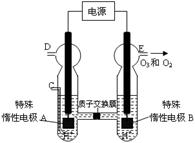
 (4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3 (g) NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是
(4)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3 (g) NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是 
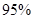 以上是以NO形式存在的,可发生反应NO(g)+ O3 (g)
以上是以NO形式存在的,可发生反应NO(g)+ O3 (g)  NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是 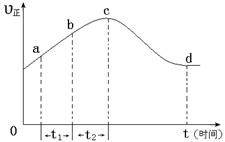
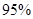 以上是以NO形式存在的,可发生反应NO(g)+ O3 (g)
以上是以NO形式存在的,可发生反应NO(g)+ O3 (g)  NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是