题目内容
8.下列化学用语或解释正确的是( )| A. | 碳酸的电离方程式:H2CO3?H++CO32- | |
| B. | 少量二氧化硫通入氢氧化钠溶液中的化学方程式:SO2+NaOH═NaHSO3 | |
| C. | 碳酸氢钠溶液显碱性:HCO3-+H2O═H3O++CO32- | |
| D. | 向小苏打溶液中加入过量的石灰水:Ca2++OH-+HCO3-═CaCO3↓+H2O |
分析 A.碳酸电离分步进行,以第一步为主;
B.反应生成亚硫酸钠和水;
C.水解生成碳酸和氢氧根离子;
D.小苏打完全反应,生成碳酸钙、水、NaOH.
解答 解:A.碳酸的电离方程式为H2CO3?H++HCO3-,故A错误;
B.少量二氧化硫通入氢氧化钠溶液中的化学方程式为SO2+2NaOH═Na2SO3+H2O,故B错误;
C.碳酸氢钠溶液显碱性,水解的离子反应为HCO3-+H2O?H2CO3+OH-,故C错误;
D.向小苏打溶液中加入过量的石灰水的离子反应为Ca2++OH-+HCO3-═CaCO3↓+H2O,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应、水解反应的离子反应考查,题目难度不大.

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
19.“化学是人类进步的关键”.下列说法正确的是( )
| A. | 用加酶洗衣粉洗衣服时,温度越高效果越好 | |
| B. | “神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃 | |
| C. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| D. | 乙二醇可用来生产聚酯纤维和作汽车发动机的抗冻剂 |
16.磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池的电极材料.某化工厂以铁红、锂辉石LiAl(SiO3)2(含少量Ca2+、Mg2+的盐)、碳粉等原料来生产磷酸亚铁锂.其主要工艺流程如图:

已知:2LiAl(SiO3)2+H2SO4(浓)$\frac{\underline{\;250~300℃\;}}{\;}$Li2SO4+Al2O3•4SiO2•H2O↓
(1)从滤渣Ⅰ中可分离出Al2O3,如下图所示.请写出生成沉淀的离子方程式Al3++3NH3•H2O=Al(OH)3↓+3NH4+.

(2)滤渣Ⅱ的主要成分是:Mg(OH)2、CaCO3(填化学式).
(3)向滤液Ⅱ中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失.
(4)写出在高温下生成磷酸亚铁锂的化学方程式2FePO4+Li2CO3+2C$\frac{\underline{\;高温\;}}{\;}$2LiFePO4+3CO↑.

已知:2LiAl(SiO3)2+H2SO4(浓)$\frac{\underline{\;250~300℃\;}}{\;}$Li2SO4+Al2O3•4SiO2•H2O↓
| 温度/℃ | 20 | 40 | 60 | 80 |
| 溶解度(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| 溶解度(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |

(2)滤渣Ⅱ的主要成分是:Mg(OH)2、CaCO3(填化学式).
(3)向滤液Ⅱ中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失.
(4)写出在高温下生成磷酸亚铁锂的化学方程式2FePO4+Li2CO3+2C$\frac{\underline{\;高温\;}}{\;}$2LiFePO4+3CO↑.
3. 醇的化学性质主要由羧基官能团所决定,如1-丁醇在银催化的条件下能与氧气反应生成正丁醛.相应醇和醛的有关物理性质如表:
醇的化学性质主要由羧基官能团所决定,如1-丁醇在银催化的条件下能与氧气反应生成正丁醛.相应醇和醛的有关物理性质如表:
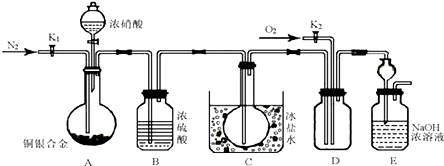
在化学工业上常用重铬酸钠的酸性溶液替代银和氧气,其模拟装置如图:
(B中为足量的重铬酸钠的酸性溶液,A中装有适量的1-丁醇和少量沸石,反应温度为93℃左右,E中为馏出物)
回答下列问题:
(1)上述装置图中,B仪器的名称是滴液漏斗,其使用前必须进行的操作是检漏.
(2)D仪器的名称是直形冷凝管,冷水应从b处进入(填a或b).
(3)实验操作过程中,若加热后发现未加沸石,则采取的正确方法是冷却后补加.
(4)将正丁醛粗产品提纯,要先进行操作Ⅰ,再进行操作Ⅱ,则操作Ⅰ是分液(填操作名称).
(5)反应温度应保持在93℃左右,其原因是既可保证正丁醛要及时蒸出,又可避免其被进一步氧化.
(6)上述装置图中,对应温度计C1、C2的放置判断正确的是c.
a.C1、C2均错误 b.C1错误C2正确 c.C1、C2均正确 d.C1正确C2错误
(7)正丁醛与新制的Cu(OH)2发生反应,该反应的化学方程式为CH3CH2CH2CHO+NaOH+2Cu(OH)2$\stackrel{△}{→}$CH3CH2CH2COONa+Cu2O↓+3H2O.
 醇的化学性质主要由羧基官能团所决定,如1-丁醇在银催化的条件下能与氧气反应生成正丁醛.相应醇和醛的有关物理性质如表:
醇的化学性质主要由羧基官能团所决定,如1-丁醇在银催化的条件下能与氧气反应生成正丁醛.相应醇和醛的有关物理性质如表:| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 1-丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
(B中为足量的重铬酸钠的酸性溶液,A中装有适量的1-丁醇和少量沸石,反应温度为93℃左右,E中为馏出物)
回答下列问题:
(1)上述装置图中,B仪器的名称是滴液漏斗,其使用前必须进行的操作是检漏.
(2)D仪器的名称是直形冷凝管,冷水应从b处进入(填a或b).
(3)实验操作过程中,若加热后发现未加沸石,则采取的正确方法是冷却后补加.
(4)将正丁醛粗产品提纯,要先进行操作Ⅰ,再进行操作Ⅱ,则操作Ⅰ是分液(填操作名称).
(5)反应温度应保持在93℃左右,其原因是既可保证正丁醛要及时蒸出,又可避免其被进一步氧化.
(6)上述装置图中,对应温度计C1、C2的放置判断正确的是c.
a.C1、C2均错误 b.C1错误C2正确 c.C1、C2均正确 d.C1正确C2错误
(7)正丁醛与新制的Cu(OH)2发生反应,该反应的化学方程式为CH3CH2CH2CHO+NaOH+2Cu(OH)2$\stackrel{△}{→}$CH3CH2CH2COONa+Cu2O↓+3H2O.
13.下列叙述正确的是( )
| A. | 原子晶体中,共价键的键能越大,熔沸点越高 | |
| B. | 分子晶体中,分子间作用力越大,该分子越稳定 | |
| C. | 金属阳离子只能与阴离子构成晶体 | |
| D. | 正四面体构型的分子中,键角一定为109°28′ |
20.今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.根据上述实验,以下推测正确的是( )
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.根据上述实验,以下推测正确的是( )
| A. | Cl- 不可能存在 | B. | 100 mL溶液中含0.01 mol CO32- | ||
| C. | K+一定存在 | D. | Ba2+一定不存在,Mg2+可能存在 |

 Fe(OH)3+3H+,过量盐酸抑制FeCl3水解(结合离子方程式简要说明).
Fe(OH)3+3H+,过量盐酸抑制FeCl3水解(结合离子方程式简要说明).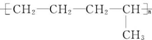 的单体是CH2═CH-CH3、CH2═CH2;(写结构简式)
的单体是CH2═CH-CH3、CH2═CH2;(写结构简式)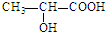 )中的官能团名称是:羟基、羧基;两分子乳酸在浓硫酸加热的条件下,可生成一种环状酯,写出此酯的结构简式:
)中的官能团名称是:羟基、羧基;两分子乳酸在浓硫酸加热的条件下,可生成一种环状酯,写出此酯的结构简式: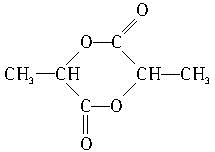 ;
;